题目内容
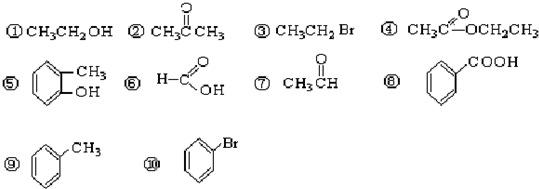
5.22.请根据官能团的不同对下列有机物进行分类:(1)属于芳香烃的⑨;(2)属于醇类的有①;
(3)属于醛的⑦;(4)属于羧酸的有⑥⑧.
分析 (1)属于芳香烃的有机物只含C、H两种元素,且含有苯环或稠环;
(2)属于醇类的物质应含有羟基,且羟基与苯环不直接相连;
(3)根据醛基的结构简式判断;
(4)属于羧酸的有机物应含有-COOH.
解答 解:(1)属于芳香烃的有机物只含C、H两种元素,且含有苯环或稠环,题中只有⑨符合,故答案为:⑨;
(2)属于醇类的物质应含有羟基,且羟基与苯环不直接相连,题中只有①符合,故答案为:①;
(3)醛基的结构简式为 ,则题中⑦含有醛基,故答案为:⑦;
,则题中⑦含有醛基,故答案为:⑦;
(4)羧基的结构简式为-COOH,则题中⑥⑧为羧酸,故答案为:⑥⑧.
点评 本题考查官能团的结构和性质,侧重于有机物化合物基础知识的考查,注意把握有机物的官能团的结构简式和有机物类别的判断,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.实验测定NaHCO3溶液显碱性,下列说法中正确的是( )
| A. | 在水溶液中,HCO3-仅仅发生水解 | |
| B. | 在水溶液中,HCO3-仅仅发生电离 | |
| C. | 在水溶液中,HCO3-的水解程度要大于电离程度 | |
| D. | 在水溶液中,HCO3-的电离程度要大于水解程度 |
4.Mg、Al、Fe分别与足量的HC1反应,产生的气体在相同状况下,均是5.6升,则Mg、Al、Fe三种金属物质的量比为( )
| A. | 3:2:2 | B. | 2:3:2 | C. | 2:2:3 | D. | 3:2:3 |
10. 苯甲酸广泛用于医药、食品、染料、化工等领域.以下是实验室制备苯甲酸的一种方法.反应原理如下:
苯甲酸广泛用于医药、食品、染料、化工等领域.以下是实验室制备苯甲酸的一种方法.反应原理如下:
 +2KMnO4$\stackrel{△}{→}$
+2KMnO4$\stackrel{△}{→}$ +2MnO2↓+KOH+H2O
+2MnO2↓+KOH+H2O
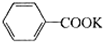 +HCl→
+HCl→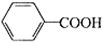 ↓+KCl
↓+KCl
相关资料:
实验步骤:
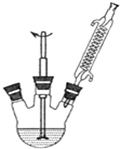
如图组装反应装置(冷凝水.夹持及加热装置未画出),并在三颈烧瓶中依次加入120mL水、9,.4g高锰酸钾和3.0mL甲苯.
②将三颈烧瓶中的混合液体搅拌,加热至沸腾,直到甲苯完全反应.
③趁热过滤反应混合物.若滤液呈紫色,则需加入适量的亚硫酸氢钠溶液至紫色褪去后再过滤,用热水洗涤滤渣,洗涤液合并至滤液中.
④用冰水冷却滤液,然后用浓盐酸酸化,过滤,用少量冷水洗涤滤渣,得到苯甲酸粗产品,经重结晶得到精制的苯甲酸.
回答下列问题:
(1)本实验应选择的三颈烧瓶规格为B(填字母序号).
A.100mL B.250mL C.500mL D.1000mL
(2)判断甲苯已完全反应的现象是三颈烧瓶中混合液不再分层、回流液不再出现油珠.
(3)实验步骤④中,用少量冷水而不用热水洗涤滤渣的目的是减少苯甲酸因溶解造成损失;苯甲酸粗产品除了可用重结晶法精制外,还可用B法.
A.蒸发 B.升华 C.过滤 D.分液
(4)精制的苯甲酸纯度测定:称取1.220g样品,用稀乙醇溶解并配成100mL溶液,分别取25,.00mL溶液,用0.1000mo1•L-1NaOH标准溶液滴定,三次滴定消耗NaOH溶液的体积分别为V1=24.70mL、V2=24.80mL、V3=25.80mL.
①配制溶液时用稀乙醇而不用蒸馏水作溶剂的原因是常温下苯甲酸微溶于水易溶于乙醇.
②若用酚酞作指示剂,确定滴定终点的现象是滴加最后一滴氢氧化钠标准溶液后,溶液由无色变为浅红色,且30秒不褪色.
③产品的纯度为99.00%.
 苯甲酸广泛用于医药、食品、染料、化工等领域.以下是实验室制备苯甲酸的一种方法.反应原理如下:
苯甲酸广泛用于医药、食品、染料、化工等领域.以下是实验室制备苯甲酸的一种方法.反应原理如下: +2KMnO4$\stackrel{△}{→}$
+2KMnO4$\stackrel{△}{→}$ +2MnO2↓+KOH+H2O
+2MnO2↓+KOH+H2O +HCl→
+HCl→ ↓+KCl
↓+KCl相关资料:
| 名称 | 相对分子质量 | 性状 | 熔点/℃ | 溶解度 | |
| 水 | 乙醇 | ||||
| 甲苯 | 92 | 无色液体易燃易挥发 | -96 | 不溶 | 易容 |
| 苯甲酸 | 122 | 白色片状或针状晶体 | 122.4 (100℃升华) | 25℃0.35g 80℃2.7g | 易容 |
如图组装反应装置(冷凝水.夹持及加热装置未画出),并在三颈烧瓶中依次加入120mL水、9,.4g高锰酸钾和3.0mL甲苯.
②将三颈烧瓶中的混合液体搅拌,加热至沸腾,直到甲苯完全反应.
③趁热过滤反应混合物.若滤液呈紫色,则需加入适量的亚硫酸氢钠溶液至紫色褪去后再过滤,用热水洗涤滤渣,洗涤液合并至滤液中.
④用冰水冷却滤液,然后用浓盐酸酸化,过滤,用少量冷水洗涤滤渣,得到苯甲酸粗产品,经重结晶得到精制的苯甲酸.
回答下列问题:
(1)本实验应选择的三颈烧瓶规格为B(填字母序号).
A.100mL B.250mL C.500mL D.1000mL
(2)判断甲苯已完全反应的现象是三颈烧瓶中混合液不再分层、回流液不再出现油珠.
(3)实验步骤④中,用少量冷水而不用热水洗涤滤渣的目的是减少苯甲酸因溶解造成损失;苯甲酸粗产品除了可用重结晶法精制外,还可用B法.
A.蒸发 B.升华 C.过滤 D.分液
(4)精制的苯甲酸纯度测定:称取1.220g样品,用稀乙醇溶解并配成100mL溶液,分别取25,.00mL溶液,用0.1000mo1•L-1NaOH标准溶液滴定,三次滴定消耗NaOH溶液的体积分别为V1=24.70mL、V2=24.80mL、V3=25.80mL.
①配制溶液时用稀乙醇而不用蒸馏水作溶剂的原因是常温下苯甲酸微溶于水易溶于乙醇.
②若用酚酞作指示剂,确定滴定终点的现象是滴加最后一滴氢氧化钠标准溶液后,溶液由无色变为浅红色,且30秒不褪色.
③产品的纯度为99.00%.
14.除去乙酸乙酯中的乙酸最好的方法是( )
| A. | 用水洗 | B. | 用盐酸洗 | ||
| C. | 用氢氧化钠溶液洗 | D. | 用饱和Na2CO3溶液 |
15.某草酸亚铁样品(FeC2O4•xH2O)中含有少量硫酸亚铁.现用滴定法测定该样品中FeC2O4的含量.滴定反应是:5Fe2++5C2O42-+3MnO4-+24H+═5Fe3++10CO2↑+3Mn2++12H2O
实验方案设计为:
①将准确称量的a g草酸亚铁样品置于250mL锥形瓶内,加入适量2mol/L的H2SO4溶液,使样品溶解,加热至70℃左右,立即用浓度为0.02000mol/L的高锰酸钾标准溶液滴定至终点,记下滴定管内液面读数为b mL
②向上述滴定混合液中加入适量的Zn粉和过量的2mol/L的H2SO4溶液,煮沸5-8min,经检验溶液合格后,继续用0.02000mol/L的高锰酸钾标准溶液滴定至终点,记下滴定管内液面读数为cmL
③重复以上实验1-2次.
④数据处理.
请回答下列问题:
(1)上述实验方案中的步骤③是重复以上实验1-2次.
(2)洁净的滴定管在滴定前必须进行的操作是:
Ⅰ.检验活塞是否漏水.
Ⅱ.用高锰酸钾标准溶液润洗滴定管.
Ⅲ.加入高锰酸钾标准溶液,赶走尖嘴部位的气泡,调节起始读数.
(3)步骤②中检验溶液是否合格的操作是:取1滴煮沸后的溶液滴入装有KSCN溶液的试管中,如溶液中没有出现血红色(或红色),则说明溶液合格.
(4)某小组的一次测定数据记录如表:
根据数据计算0.1970g 样品中:n(Fe2+)═0.001110mol; n(C2O42-)═0.001010mol;FeC2O4 的质量分数为73.81%(精确到0.01%).
实验方案设计为:
①将准确称量的a g草酸亚铁样品置于250mL锥形瓶内,加入适量2mol/L的H2SO4溶液,使样品溶解,加热至70℃左右,立即用浓度为0.02000mol/L的高锰酸钾标准溶液滴定至终点,记下滴定管内液面读数为b mL
②向上述滴定混合液中加入适量的Zn粉和过量的2mol/L的H2SO4溶液,煮沸5-8min,经检验溶液合格后,继续用0.02000mol/L的高锰酸钾标准溶液滴定至终点,记下滴定管内液面读数为cmL
③重复以上实验1-2次.
④数据处理.
请回答下列问题:
(1)上述实验方案中的步骤③是重复以上实验1-2次.
(2)洁净的滴定管在滴定前必须进行的操作是:
Ⅰ.检验活塞是否漏水.
Ⅱ.用高锰酸钾标准溶液润洗滴定管.
Ⅲ.加入高锰酸钾标准溶液,赶走尖嘴部位的气泡,调节起始读数.
(3)步骤②中检验溶液是否合格的操作是:取1滴煮沸后的溶液滴入装有KSCN溶液的试管中,如溶液中没有出现血红色(或红色),则说明溶液合格.
(4)某小组的一次测定数据记录如表:
| a/g | 起始读数/mL | b/mL | c/mL |
| 0.1970 | 0.00 | 31.30 | 42.40 |
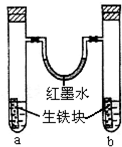 如图装置中,U型管内为红墨水,a,b试管内分别盛有是食盐水和醋酸溶液,各加入生铁快,放置右方时间,请回答下列问题:
如图装置中,U型管内为红墨水,a,b试管内分别盛有是食盐水和醋酸溶液,各加入生铁快,放置右方时间,请回答下列问题: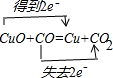 .
.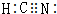 ,其中Y原子的杂化方式是sp,ZW3-的空间构型为平面三角形.
,其中Y原子的杂化方式是sp,ZW3-的空间构型为平面三角形.