题目内容
9.下列物质是烷烃的是( )| A. | CH2Br-CH2Br | B. | C5H11OH | C. | C100H202 | D. | C6H6 |
分析 烷烃是碳原子之间以碳碳单键结合,符合通式CnH2n+2,据此分析.
解答 解:A.CH2Br-CH2Br含有溴元素,不属于烃,故A错误;
B.C5H11OH含有氧元素,不属于烃,故B错误;
C.C100H202符合CnH2n+2,属于烷烃,故C正确;
D.C6H6不符合CnH2n+2,不属于烷烃,故D错误.
故选C.
点评 本题考查了烷烃通式在确定烷烃分子式时的应用,旨在巩固学生的基础,明确烷烃的通式是答题的根据,难度不大.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
3.用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,1 mol CO2、CO的混合气中含有的氧原子数为1.5NA | |
| B. | 常温常压下,11.2 L 氯化氢气体中含有的分子数为0.5NA | |
| C. | NA个甲烷分子和1mol甲烷的质量相等 | |
| D. | 1 mol•L-1 CuCl2溶液中含有的氯离子数为2NA |
4.Mg、Al、Fe分别与足量的HC1反应,产生的气体在相同状况下,均是5.6升,则Mg、Al、Fe三种金属物质的量比为( )
| A. | 3:2:2 | B. | 2:3:2 | C. | 2:2:3 | D. | 3:2:3 |
4.下列反应需要加入还原剂才能实现的是( )
| A. | MnO4-→Mn2+ | B. | Cl-→Cl2 | C. | HCO3-→CO2 | D. | PCl5→H3PO4 |
14.除去乙酸乙酯中的乙酸最好的方法是( )
| A. | 用水洗 | B. | 用盐酸洗 | ||
| C. | 用氢氧化钠溶液洗 | D. | 用饱和Na2CO3溶液 |
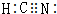 ,其中Y原子的杂化方式是sp,ZW3-的空间构型为平面三角形.
,其中Y原子的杂化方式是sp,ZW3-的空间构型为平面三角形. ,其中的化学键属于共价键(填“离子”或“共价”).
,其中的化学键属于共价键(填“离子”或“共价”).