题目内容
3.粒子甲与粒子乙在溶液中的转化关系如图所示,粒子甲不可能是( )
| A. | NH4+ | B. | Al2O3 | C. | HCO3- | D. | SO2 |
分析 A.NH4+与OH-反应生成NH3,NH3和氢离子反应生成铵根离子;
B.Al2O3与与OH-反应生成AlO2-,与氢离子反应生成Al(OH)3沉淀或铝离子;
C.HCO3-与氢氧根能反应生成CO32-,CO32-和少量H+反应可生成HCO3-;
D.SO2与氢氧根能反应生成亚硫酸根,亚硫酸根和氢离子反应生成水和SO2.
解答 解:A.NH4+与OH-反应生成NH3和H2O,NH3和氢离子反应生成铵根离子,符合转化关系,故A不选;
B.Al2O3与与OH-反应生成AlO2-,与氢离子反应生成Al(OH)3沉淀或铝离子,得不到Al2O3,不符合转化关系,故B选;
C.HCO3-与氢氧根能反应生成CO32-,CO32-和少量H+反应可发生反应:CO32-+H+═HCO3-,符合转化关系,故C不选;
D.SO2与氢氧根能反应生成亚硫酸根,亚硫酸根和氢离子反应生成水和SO2,符合转化关系,故D不选;
故选B.
点评 本题考查无机物的推断,属于验证型题目,把握物质的性质及图中转化关系为解答的关键,注意微粒之间发生的反应,题目难度不大.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
13.下列离子方程式错误的是( )
| A. | 向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| B. | 向Ca(HCO3)2溶液中滴加少量NaOH溶液:Ca2++HCO3-+OH-═CaCO3↓+H2O | |
| C. | 等物质的量的MgCl2、Ba(OH)2、HCl三种溶液混合:Mg2++2OH-═Mg(OH)2↓ | |
| D. | 氢氧化钠溶液中通入氯气:Cl2+2OH-═ClO-+Cl-+H2O |
14.下列说法正确的是( )
| A. | 232Th 转换成233U是化学变化,233U和235U的化学性质几乎相同 | |
| B. | 防止自行车钢架生锈主要是利用了电化学防腐原理 | |
| C. | 血液透析是利用了胶体的聚沉性质 | |
| D. | 葡萄酒中含有的微量的二氧化硫具有抗氧化剂作用 |
11.一定浓度的盐酸和氨水混合后形成的混合溶液中,下列说法正确的是( )
| A. | 当溶液中c(Cl-)>c(NH4+)时,Mg2+、Na+、SO32-、NO3-可以大量共存 | |
| B. | 当溶液中c(Cl-)=c(NH4+)时,Na+、CH3CH2OH、[Ag(NH3)2]+可以大量共存 | |
| C. | 当溶液中c(Cl-)<c(NH4+)时,可以发生ClO-+Cl-+2H+═Cl2+H2O | |
| D. | 若溶液中c(Cl-)=c(NH4+)时,则盐酸和氨水按物质的量1:1混合 |
18.水的电离平衡曲线如如图所示,下列说法不正确的是( )
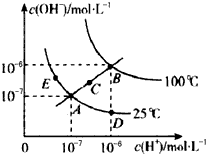

| A. | 图中五点Kw间的关系:B>C>A=D=E | |
| B. | 若从A点到D点,可采用在水中加入少量酸的方法 | |
| C. | 若从A点到C点,在温度不变时向水中加入适量NH4Cl固体 | |
| D. | 若处在B点时,将pH=2的硫酸与pH=10的KOH溶液等体积混合后,溶液显中性 |
8.下列各组物质属于同系物的是( )
| A. | H2和D2 | B. | 苯和甲苯 | C. | 正丁烷和异丁烷 | D. | 葡萄糖和果糖 |
15.150mL浓度为3mol•L-1的盐酸跟过量的锌片反应,为加快反应速率又不影响生成氢气的总量,可采用的方法是
( )
( )
| A. | 加入适量的6mol•L-1的盐酸 | B. | 加入数滴氯化铜溶液 | ||
| C. | 加入数滴硝酸铜溶液 | D. | 加入适量的氯化钠溶液 |
12.元素性质随原子序数的递增呈周期性变化的实质是( )
| A. | 元素的相对原子质量增大,量变引起质变 | |
| B. | 原子的电子层数增多 | |
| C. | 原子核外电子排布呈周期性变化 | |
| D. | 原子半径呈周期性变化 |
1.配制250mL 0.10mol/L的NaOH溶液时,下列实验操作会使配得的溶液中NaOH物质的量浓度偏大的是( )
| A. | 转移溶液后未洗涤烧杯和玻璃棒就直接定容 | |
| B. | 称量时,在天平托盘上放上称量纸,将NaOH固体放在纸上称量 | |
| C. | 在容量瓶中进行定容时俯视刻度线 | |
| D. | 定容后把容量瓶倒置摇匀,发现液面低于刻度线,又补足了所缺的水 |