题目内容
18.水的电离平衡曲线如如图所示,下列说法不正确的是( )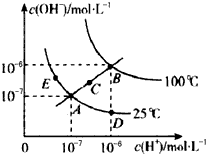
| A. | 图中五点Kw间的关系:B>C>A=D=E | |
| B. | 若从A点到D点,可采用在水中加入少量酸的方法 | |
| C. | 若从A点到C点,在温度不变时向水中加入适量NH4Cl固体 | |
| D. | 若处在B点时,将pH=2的硫酸与pH=10的KOH溶液等体积混合后,溶液显中性 |
分析 A、ADE都处于25℃时,Kw相等,然后比较B、E两点的c(H+)和c(OH-)的大小,依次比较Kw的大小;
B、从A点到D点c(H+)变大,但c(OH-)变小,温度不变,Kw不变;
C、从A点到C点c(H+)和c(OH-)的变化判断Kw的变化,依次判断温度的变化;
D、根据B点时Kw计算酸与碱溶液中c(H+)和c(OH-),然后判断溶液的酸碱性.
解答 解:A、ADE都处于25℃时,Kw相等,B点c(H+)和c(OH-)都大于E点的c(H+)和c(OH-),并且C点的c(H+)和c(OH-)大于A点c(H+)和c(OH-),c(H+)和c(OH-)越大,Kw越大,故B>C>A=D=E,故A正确;
B、加酸,c(H+)变大,但c(OH-)变小,但温度不变,Kw不变,故B正确;
C、若从A点到C点,c(H+)变大,c(OH-)变大,Kw增大,温度应升高,故C错误;
D、若处在B点时,Kw=1×10-12,pH=2的硫酸中c(H+)=10-2mol/L,pH=10的KOH中c(OH-)=10-2mol•L-1,等体积混合,恰好中和,溶液显中性,故D正确;故选C.
点评 本题考查水的电离平衡移动问题,结合图象判断并分析溶液在不同温度下的Kw,做题时注意根据图象比较c(H+)和c(OH-)的大小.

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
9.有机物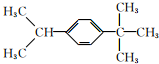 的一氯化物共有(不考虑立体异构)( )
的一氯化物共有(不考虑立体异构)( )
 的一氯化物共有(不考虑立体异构)( )
的一氯化物共有(不考虑立体异构)( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 7种 |
6.符合下列条件的有机物中,同分异构体(不考虑立体异构)数目最多的是( )
| A. | 分子式为C5H10且能使溴的CCl4溶液褪色 | |
| B. | 分子式为C7H16且含有三个甲基 | |
| C. | 分子式为C4H8O2且能与NaOH溶液反应 | |
| D. | 分子式为C4H10O且能与钠反应 |
13.下列说法正确的是( )
| A. | 氧化钠、氧化铁、氧化镁均为碱性氧化物 | |
| B. | 离子键、共价键、金属键、氢键均为化学键 | |
| C. | 氨水、水玻璃、水银、聚乙烯均为混合物 | |
| D. | 水能、风能、生物质能、核能均为可再生能源 |
3.粒子甲与粒子乙在溶液中的转化关系如图所示,粒子甲不可能是( )


| A. | NH4+ | B. | Al2O3 | C. | HCO3- | D. | SO2 |
10.化学与人类生活密切相关,下列说法正确的是( )
| A. | 硅胶可用作食品干燥剂 | |
| B. | 氢氧化铝和氢氧化钠都是常见的胃酸中和剂 | |
| C. | 生活中使用的合成纤维和光导纤维都是有机物 | |
| D. | PM2.5中含有的铅、镉、砷等有害元素都是金属元素 |
7.在光照条件下CH4和Cl2反应,不可能生成的物质是( )
| A. | H2 | B. | HCl | C. | CH3Cl | D. | CCl4 |
8.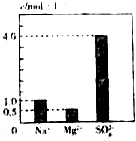 0.5L的溶液中含有Na+、Mg2+、Al3+和SO42-四种离子,其中Na+、Mg2+和SO42-的浓度大小如图所示,则下列有关说法错误的是( )
0.5L的溶液中含有Na+、Mg2+、Al3+和SO42-四种离子,其中Na+、Mg2+和SO42-的浓度大小如图所示,则下列有关说法错误的是( )
 0.5L的溶液中含有Na+、Mg2+、Al3+和SO42-四种离子,其中Na+、Mg2+和SO42-的浓度大小如图所示,则下列有关说法错误的是( )
0.5L的溶液中含有Na+、Mg2+、Al3+和SO42-四种离子,其中Na+、Mg2+和SO42-的浓度大小如图所示,则下列有关说法错误的是( )| A. | 该溶液中NaSO4的物质的量浓度为1.0mol•L-1 | |
| B. | 该溶液中MgSO4的物质的量为0.25mol | |
| C. | 该溶液中MgSO4的质量为30g | |
| D. | 该溶液中Al2(SO4)3的物质的量浓度为1.0mol•L-1 |