题目内容
13.下列叙述中正确的是( )| A. | 金属的熔点和沸点都很高 | |
| B. | H2O、CCl4都是含有极性键的非极性分子 | |
| C. | HF、HCl、HBr、HI的酸性依次增强 | |
| D. | H2O是一种非常稳定的化合物,这是由于氢键所致 |
分析 A.金属晶体的熔沸点,有的很高,有的很低;
B.H2O是极性分子;
C.非金属性越强,氢化物越稳定,酸性越弱;
D.由于水分子中O-H键稳定,水是稳定的化合物.
解答 解:A.金属晶体的熔沸点,有的很高,如W,有的很低,如Na,故A错误;
B.CCl4是正四面体结构,分子中正负电荷重心重合,是由极性键的非极性分子,而H2O为V型结构,分子中正负电荷重心不重合,属于极性分子,故B错误;
C.由于非金属性F>Cl>Br>I,故H-X键稳定性减弱,HX中氢离子的电离程度逐渐增大,酸性增强,故C正确;
D.水分子间存在氢键,影响其物理性质,而水的稳定性是化学键的表现,故D错误.
故选C.
点评 本题主要考查熔沸点比较、分子极性、化学键与氢键等,理解掌握规律是解题的关键,难度不大.

练习册系列答案
相关题目
3.下列说法错误的是( )
| A. | 水玻璃可用于制备硅胶和木材防火剂 | |
| B. | 在现代化学工业中催化剂的应用十分普遍,对于给定条件下反应物之间能够同时发生多个反应时,理想催化剂还可以大幅度提高目标产物在最终产物中的比率 | |
| C. | 煤经过气化和液化两个物理变化过程,可变为清洁能源 | |
| D. | PM2.5是指大气中直径小于或等于2.5微米的颗粒物,也称为“细颗粒物”,PM2.5分散在空气中可能形成胶体或浊液 |
4.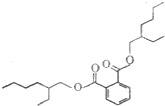 塑化剂是工业上被广泛使用的高分子材料添加剂,食用后对人体有害,其结构式如图.下列有关塑化剂的说法正确的是( )
塑化剂是工业上被广泛使用的高分子材料添加剂,食用后对人体有害,其结构式如图.下列有关塑化剂的说法正确的是( )
 塑化剂是工业上被广泛使用的高分子材料添加剂,食用后对人体有害,其结构式如图.下列有关塑化剂的说法正确的是( )
塑化剂是工业上被广泛使用的高分子材料添加剂,食用后对人体有害,其结构式如图.下列有关塑化剂的说法正确的是( )| A. | 易溶于水,其水溶液有丁达尔效应 | B. | 在稀硫酸中不能稳定存在 | ||
| C. | 不能发生还原反应 | D. | 不能发生氧化反应 |
8.下列关于物质性质变化的比较中正确的( )
①酸性:HClO4>HBrO4>HIO4
②碱性:Ba(OH)2>Ca(OH)2>Mg(OH)2
③热稳定性:HCl>H2S>PH3
④还原性:F->Cl->Br-.
①酸性:HClO4>HBrO4>HIO4
②碱性:Ba(OH)2>Ca(OH)2>Mg(OH)2
③热稳定性:HCl>H2S>PH3
④还原性:F->Cl->Br-.
| A. | ①②④ | B. | ②③④ | C. | ①②③ | D. | ①②③④ |
5.下列各组所有的元素组合,既可以构成离子晶体,又可以构成分子晶体的是( )
| A. | S.O.K | B. | Na.C.O | C. | H.O.S | D. | H.N.O |
3.(CH3CH2)2CHCH3的正确命名是( )
| A. | 2-乙基丁烷 | B. | 2-甲基戊烷 | C. | 3-甲基戊烷 | D. | 3-乙基丁烷 |
 一种锌锰干电池外壳的纸层包装印有如图所示的文字,其电极分别为碳棒和锌皮,以糊状NH4Cl和ZnCl2作电解质(其中加人MnO2氧化吸收H2)
一种锌锰干电池外壳的纸层包装印有如图所示的文字,其电极分别为碳棒和锌皮,以糊状NH4Cl和ZnCl2作电解质(其中加人MnO2氧化吸收H2) .
.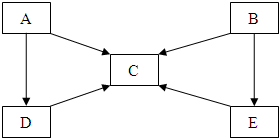 A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如图所示.其中A、B、C、D、E在常温下都是气体,B为红棕色.
A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如图所示.其中A、B、C、D、E在常温下都是气体,B为红棕色.