题目内容
3.下列说法错误的是( )| A. | 水玻璃可用于制备硅胶和木材防火剂 | |
| B. | 在现代化学工业中催化剂的应用十分普遍,对于给定条件下反应物之间能够同时发生多个反应时,理想催化剂还可以大幅度提高目标产物在最终产物中的比率 | |
| C. | 煤经过气化和液化两个物理变化过程,可变为清洁能源 | |
| D. | PM2.5是指大气中直径小于或等于2.5微米的颗粒物,也称为“细颗粒物”,PM2.5分散在空气中可能形成胶体或浊液 |
分析 A.硅酸钠具有粘性,可用来制备硅胶,硅酸盐不燃烧,可做木材防火剂的原料;
B.催化剂会影响目标产物在最终产物中的比例;
C.煤经过气化和液化生成了可燃性气体或液体;
D.分散质粒子直径在1nm~100nm(0.001微米~0.1微米)之间的分散系属于胶体,大于100nm的属于浊液.
解答 解:A.水玻璃为硅酸钠的水溶液,具有粘性,可用来制备硅胶,硅酸盐不燃烧,可做木材防火剂的原料,故A正确;
B.催化剂只能对主反应即生成目标产物的那个反应起起作用,这样在转化率一定的时候的确目标产物的比例会加大,故B正确;
C.煤经过气化和液化生成了可燃性气体或液体,变为清洁能源,是化学变化,故C错误;
D.PM2.5的直径小于或等于2.5微米的颗粒物,当颗粒直径在(0.001微米~0.1微米)之间分散于空气形成的就是胶体,故D正确;
故选:C.
点评 本题为综合题,考查了物质的用途、催化剂的作用、物理变化与化学变化的区别、胶体的判断,明确胶体的分散质粒度大小是解题关键,题目难度不大.

练习册系列答案
相关题目
13.根据现象分析,所得结论正确的是( )


| 选项 | 实验现象 | 结论 |
| A | 左烧杯中铁表面有气泡,右边烧杯中铜表面有气泡 | 活动性:Al>Fe>Cu |
| B | 左边棉花变为橙色,右边棉花变为蓝色 | 还原性:I->Br+>Cl- |
| C | 开始铜粉不溶解,溶液呈无色,后有气体放出,溶液呈蓝色 | 氧化性:NaNO3>H2SO4>Cu2+ |
| D | 锥形瓶中有气体产生,烧杯中液体变浑浊 | 非金属性:Cl>C>Si |
| A. | A | B. | B | C. | C | D. | D |
14.常温下,下列各组离子一定能大量共存的是( )
| A. | pH=1的溶液中:Na+、Cl-、K+、HS- | |
| B. | 水电离出的c(H+)=10-12mol/L中:Ba2+、K+、Cl-、CO32- | |
| C. | $\frac{c(O{H}^{-})}{c({H}^{+})}$=1012的水溶液中:CH3COO-、CO32-、Na+、K+ | |
| D. | c(Al3+)=1mol/L的溶液中:Na+、NO3-、SO42-、HCO3- |
18.下列各项中表达正确的是( )
| A. | F-的结构示意图: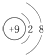 | B. | CH4分子的比例模型: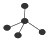 | ||
| C. | CCl4的电子式: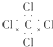 | D. | 乙烯的结构简式:CH2CH2 |
8.25时,将不同浓度的二元弱酸H2A和NaOH溶液等体积混合(体积变化忽略不计),测得反应后溶液的pH如下表:下列判断不正确的是( )
| 实验编号 | 起始浓度/mol•L-1 | 反应后溶液的pH | |
| c(H2A) | c(NaOH) | ||
| ① | X | 0.10 | 9 |
| ② | 0.10 | 0.10 | 5 |
| A. | X<0.1 | |
| B. | HA-的电离程度大于水解程度 | |
| C. | 将实验①所得溶液加水稀释后,$\frac{c({A}^{2-})}{c(H{A}^{-})}$变大 | |
| D. | 实验②所得溶液:c(Na+)=c(A2-)+c(HA-)+c(H2A) |
15.对可逆反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列叙述正确的是( )
| A. | 化学反应速率关系是:3υ(NH3)═2υ(H2O) | |
| B. | 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 | |
| C. | 达到化学平衡时,若增加容器体积,则正反应速率减少,逆反应速率增大 | |
| D. | 达到化学平衡时,5υ正(O2)=4υ逆(NO) |
12.能说明乙醇的结构简式是CH3CH2OH而不是CH3OCH3的事实是( )
| A. | 乙醇能够燃烧 | |
| B. | 乙醇(一定量)与足量金属钠反应放出氢气的量 | |
| C. | 乙醇的分子式是C2H6O | |
| D. | 乙醇的沸点比水的低、密度比水的小 |
13.下列叙述中正确的是( )
| A. | 金属的熔点和沸点都很高 | |
| B. | H2O、CCl4都是含有极性键的非极性分子 | |
| C. | HF、HCl、HBr、HI的酸性依次增强 | |
| D. | H2O是一种非常稳定的化合物,这是由于氢键所致 |
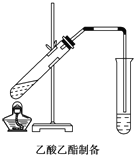 如图,在左试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2mL乙酸,充分摇匀.按图连接好装置,用酒精灯对左试管小火加热3~5min后,改用大火加热,当观察到右试管中有明显现象时停止实验.
如图,在左试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2mL乙酸,充分摇匀.按图连接好装置,用酒精灯对左试管小火加热3~5min后,改用大火加热,当观察到右试管中有明显现象时停止实验.