题目内容
【题目】现有前四周期原子序数依次递增的五种元素A、B、C、D、E。 A、D元素基态原子中成对电子数是未成对电子数的3倍,且D元素基态原子中有6个未成对电子;B的基态原子核外只有7个原子轨道填充了电子,B、C元素基态原子的3p能级上均有1个未成对电子;E元素排在周期表的15列。
(1)B元素基态原子核外电子有_______种运动状态,电子占据的最高能层符号为_______,该能层具有的原子轨道数为_______、电子数为_____。
(2)C、E两元素可以形成化合物EC3,此化合物的VSEPR模型为_______,是_______分子(填“极性”、“非极性”)。
(3)写出D基态原子的外围电子排布图____________。
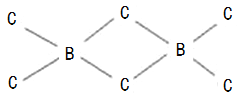
(4)B、C两元素也可以形成共价化合物BC3,但BC3经常以二聚(B2C6)的形式存在,二聚分子具有配位键,分子中原子间成键的关系如下图所示.请将图中,你认为是配位键的斜线上加上箭头。
【答案】(1)13;M;9;3
(2)四面体形;极性
(3)![]()
(4)![]() 或者
或者![]()
【解析】试题分析:(1)B元素是13号铝,基态原子核外电子有 13种运动状态,电子占据的最高能层符号为M,该能层具有的原子轨道数为9、电子数为3,故答案为:13;M;9;3;
(2)氯、砷两元素可以形成化合物AsCl3,As是sp3杂化,所以化合物的VSEPR模型为四面体形,是极性分子,故答案为:四面体形;极性;
(3)铬基态原子的外围电子排布图为:![]() ,故答案为:
,故答案为:![]() ;
;
(4)C原子最外层有4个电子,只能与B原子各提供1个电子形成一个共价键,使自己达到8电子稳定结构,而B原子最外层有3个电子,可分别与3个C原子形成共价键,因而C原子与2个B原子形成的化学键中,必有1个是配位键,由于电子对由C原子提供,这样C原子最外层电子数仍为8,B原子最外层也成为8电子结构,如图所示:![]() 或者
或者![]() ,故答案为:
,故答案为:![]() 或者
或者![]() 。
。