题目内容
2.在64g氧气中,所有氧原子的最外层电子数共有24NA个,含有质子的物质的量为32mol.分析 结合n=$\frac{m}{M}$及O2是双原子分子,氧原子最外层6个电子,氧原子的质子数为8,来分析计算.
解答 解:64g氧气的物质的量为$\frac{64g}{32g/mol}$=2mol,由O2的构成可知,氧原子的物质的量为2mol×2=4mol,所有氧原子的最外层电子数共有4mol×6=24mol,则电子数为:24NA;质子的物质的量为:4mol×8=32mol;故答案为:24NA;32mol.
点评 本题考查物质的量的计算,为高频考点,把握物质的量的有关计算公式及分子构成为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
相关题目
12.利用化学反应Fe+CuSO4═FeSO4+Cu设计原电池,下列有关描述正确的是( )
| A. | Fe为正极 | B. | Cu为负极 | ||
| C. | 负极发生还原反应 | D. | 电解质溶液是CuSO4溶液 |
13.元素是组成世界万物的基本成分,下列关于元素的说法不正确的是( )
| A. | 氯原子和氯离子都属于氯元素 | |
| B. | 合金中一定含有金属元素 | |
| C. | 人体缺铁元素会引起贫血 | |
| D. | 碳和碘元素都是人体不可缺少的微量元素 |
14.10g含有杂质的CaCO3和足量的盐酸反应,产生的CO2 0.1mol,则此样品中可能含有的杂质是( )
| A. | KHCO3和MgCO3 | B. | MgCO3和SiO2 | C. | K2CO3和 SiO2 |
2.下列反应不属于氧化还原反应的是( )
| A. | 碳酸氢钠受热分解 | B. | 铝和三氧化二铁高温下反应 | ||
| C. | 过氧化钠与水反应 | D. | 铜和浓硫酸反应 |
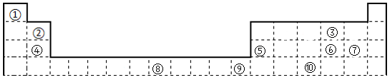
 .元素⑨的基态原子的价电子排布式为1s22s22p63s23p63d104s2.
.元素⑨的基态原子的价电子排布式为1s22s22p63s23p63d104s2.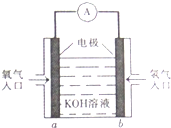 被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点.如图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从a、b两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题:
被誉为改变未来世界的十大新科技之一的燃料电池具有无污染、无噪音、高效率的特点.如图为氢氧燃料电池的结构示意图,电解质溶液为KOH溶液,电极材料为疏松多孔石墨棒.当氧气和氢气分别连续不断地从a、b两极通入燃料电池时,便可在闭合回路中不断地产生电流.试回答下列问题: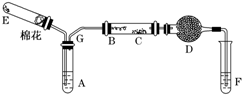 如图所示为某化学兴趣小组设计的乙醇氧化的实验装置(图中加热仪器、铁架台、铁夹等均未画出).图中,A为无水乙醇(沸点为78℃),B为绕成螺旋状的细铜丝或银丝,C为无水硫酸铜粉末,D为碱石灰,F为新制的Cu(OH)2悬浊液.(提示:乙醇催化氧化产物与新制Cu(OH)2悬浊液共热有砖红色沉淀生成)
如图所示为某化学兴趣小组设计的乙醇氧化的实验装置(图中加热仪器、铁架台、铁夹等均未画出).图中,A为无水乙醇(沸点为78℃),B为绕成螺旋状的细铜丝或银丝,C为无水硫酸铜粉末,D为碱石灰,F为新制的Cu(OH)2悬浊液.(提示:乙醇催化氧化产物与新制Cu(OH)2悬浊液共热有砖红色沉淀生成)