题目内容
7.在一定条件下,PbO2与浓盐酸反应的产物Cl2和Pb2+,则生成0.1mol Cl2所需PbO2的物质的量为0.1mol.分析 发生反应:PbO2+4HCl(浓)=PbCl2+Cl2↑+2H2O,根据方程式计算需要PbO2的物质的量.
解答 解:发生反应:PbO2+4HCl(浓)=PbCl2+Cl2↑+2H2O,可知n(PbO2)=n(Cl2)=0.1mol,故答案为:0.1mol.
点评 本题考查化学方程式有关计算,明确发生的反应是解题关键,比较基础.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.下面能说明甲比乙的非金属性强的是( )
①甲比乙容易与H2化合;
②甲单质能与乙的阴离子发生氧化还原反应
③甲的氧化物对应的水化物酸性比乙的氧化物对应的水化物酸性强;
④与某金属反应时甲原子得电子数目比乙的多;
⑤甲的氢化物比乙的氢化物稳定.
①甲比乙容易与H2化合;
②甲单质能与乙的阴离子发生氧化还原反应
③甲的氧化物对应的水化物酸性比乙的氧化物对应的水化物酸性强;
④与某金属反应时甲原子得电子数目比乙的多;
⑤甲的氢化物比乙的氢化物稳定.
| A. | ①④ | B. | ③⑤ | C. | ①②⑤ | D. | ①②④⑤ |
15.电池是人类生产和生活中的重要的能量来源,各式各样电池的发明是化学对人类的一项重大贡献.下列有关电池的叙述正确的是( )
| A. | 构成电池的两极必须是活泼性不同的金属 | |
| B. | 锌锰干电池工作时,电池内部的电流方向由碳棒流向锌桶 | |
| C. | 甲醇燃料电池工作时,甲醇在负极发生氧化反应 | |
| D. | 银锌纽扣电池工作时,电子由锌极流出经过溶液后流向银极 |
12.下列实验设计不能达到实验目的是( )
| 选项 | 实验设计 | 实验目的 |
| A | 过氧化钠与水反应 | 制备少量干燥的氧气 |
| B | 取铁在氧气中充分燃烧后的固体产物溶于稀硫酸,加KSCN溶液 | 检验铁的燃烧产物中含+3价铁 |
| C | 分别取大小相近的钠粒、钾粒投入水中,观察反应的剧烈程度 | 比较钠、钾的还原性强弱 |
| D | 取一定量铝粉分成四等份,一份铝与适量烧碱恰好完全反应,另三份铝与稀硫酸恰好完全反应,再将溶液混合、过滤、洗涤、干燥 | 制备氢氧化铝且原子利用率较高 |
| A. | A | B. | B | C. | C | D. | D |
19.下列化学用语中正确的是( )
| A. | 乙烯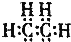 | B. | 乙基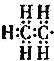 | C. | 四氯化碳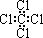 | D. | 2-甲基丙烯 |
6.一定量的乙醛发生银镜反应,析出银21.6g.等量的此醛完全燃烧时,生成的水为( )
| A. | 5.4g | B. | 3.6g | C. | 1.8g | D. | 2.4g |
7.下列物质按纯净物、混合物、电解质、非电解质的顺序组合的一组为( )
| 纯净物 | 混合物 | 电解质 | 非电解质 | |
| A | 蒸馏水 | 氨水 | 氧化铝 | 二氧化硫 |
| B | 盐酸 | 空气 | 硫酸 | 干冰 |
| C | 胆矾 | 盐酸 | 铁 | 碳酸钙 |
| D | 生石灰 | 硫酸 | 氯化铜 | 碳酸钠 |
| A. | A | B. | B | C. | C | D. | D |
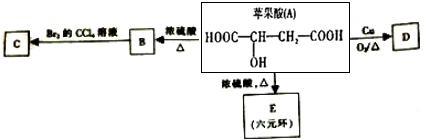
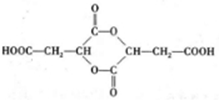 .
. 、
、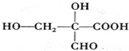 (任一种).
(任一种).