题目内容
1.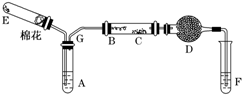 如图所示为某化学兴趣小组设计的乙醇氧化的实验装置(图中加热仪器、铁架台、铁夹等均未画出).图中,A为无水乙醇(沸点为78℃),B为绕成螺旋状的细铜丝或银丝,C为无水硫酸铜粉末,D为碱石灰,F为新制的Cu(OH)2悬浊液.(提示:乙醇催化氧化产物与新制Cu(OH)2悬浊液共热有砖红色沉淀生成)
如图所示为某化学兴趣小组设计的乙醇氧化的实验装置(图中加热仪器、铁架台、铁夹等均未画出).图中,A为无水乙醇(沸点为78℃),B为绕成螺旋状的细铜丝或银丝,C为无水硫酸铜粉末,D为碱石灰,F为新制的Cu(OH)2悬浊液.(提示:乙醇催化氧化产物与新制Cu(OH)2悬浊液共热有砖红色沉淀生成)(1)加热E处固体,目的是制取O2,若E处是KMnO4,试写出反应的化学方程式:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(2)为了使A中的乙醇平稳汽化成蒸气,可采用的加热方法是将试管A放入78℃(或略高于78℃)热水浴中;D处使用碱石灰的作用是防止F中的水蒸气与C处的无水硫酸铜反应而干扰实验结果
(3)能证明乙醇反应后的产物的实验现象是C处无水硫酸铜粉末变成蓝色,F处产生砖红色沉淀.
(4)图中G处导管倾斜的作用是使冷凝了的乙醇回流到A试管中.
分析 (1)根据实验目的分析E装置的作用,高锰酸钾受热分解为锰酸钾、二氧化锰、和氧气;
(2)根据水浴加热和直接加热的区别及实验目的分析;碱石灰有吸水的作用,据此分析;
(3)水能使无水硫酸铜变蓝;在加热条件下,乙醛和新制的Cu(OH)2悬浊液生成砖红色氧化亚铜沉淀;
(4)根据导管G具有冷凝回流的作用进行解答.
解答 解:(1)乙醇和铜不反应,和氧化铜反应,所以要先制取氧化铜;铜和氧气在加热条件下才反应生成氧化铜,需先加热制取氧气,所以加热E处固体目的制取氧气,
E处是KMnO4,高锰酸钾受热分解为锰酸钾、二氧化锰、和氧气,反应方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
故答案为:制取O2;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(2)直接加热时,生成乙醇蒸汽的速率较大,乙醇和氧化铜反应不完全,造成资源浪费,为了使A中的乙醇平稳气化成蒸气,可采用水浴加热的方法,将试管A放入78℃(或略高于78℃)热水浴中;乙醇和氧化铜反应生成乙醛、铜和水,加热F处时,F装置中的水蒸气也使无水硫酸铜变蓝,所以对乙醇和氧化铜反应生成的水蒸气造成干扰,所以D装置目的是吸收F装置中的水蒸气,防止F处产生的水蒸气对无水硫酸铜产生影响.
故答案为:将试管A放入78℃(或略高于78℃)热水浴中; 防止F中的水蒸气与C处的无水硫酸铜反应而干扰实验结果;
(3)水能使无水硫酸铜变蓝;在加热条件下,乙醛和新制的Cu(OH)2悬浊液生成砖红色氧化亚铜沉淀,如果C处无水硫酸铜变蓝,加热煮沸F,生成砖红色沉淀,说明乙醇被氧化后的产物是水和乙醛,
故答案为:C处无水硫酸铜粉末变成蓝色,F处产生砖红色沉淀;
(4)装置中G导管倾斜,能够使乙醇蒸气冷凝回流到A试管中,
故答案为:使冷凝了的乙醇回流到A试管中.
点评 本题考查了乙醇的催化氧化实验,题目难度不大,注意掌握物质性质和实验基本操作方法是解题本题关键,明确乙醇的催化氧化原理.

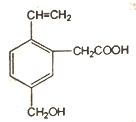
| A. | 能使酸性KMn04溶液褪色 | B. | 能发生酯化反应 | ||
| C. | 能与NaOH溶液反应 | D. | 能发生水解反应 |
| A. | 乙烯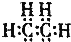 | B. | 乙基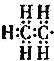 | C. | 四氯化碳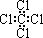 | D. | 2-甲基丙烯 |
| A. | 5.4g | B. | 3.6g | C. | 1.8g | D. | 2.4g |
| A. | 碳酸钙溶于稀盐酸中:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 稀盐酸与铁粉反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 把铜片放入硝酸银溶液中:Cu+Ag+═Cu2++Ag | |
| D. | 氢氧化钡溶液与稀H2SO4反应:Ba2++SO42-═BaSO4↓ |
| A. | 电池放电时,H2参与负极反应,发生氧化反应 | |
| B. | 电池放电时,镍元素被氧化 | |
| C. | 电池放电时,电子从氢气这一极到NiO(OH) 这一极 | |
| D. | 电池充电时,电能转化为化学能 |
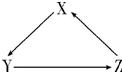 X、Y、Z为中学化学常见物质,其转化关系如下图所示(“→”表示一步转化).下列组合不正确的是( )
X、Y、Z为中学化学常见物质,其转化关系如下图所示(“→”表示一步转化).下列组合不正确的是( )| 选项 | X | Y | Z |
| A | Al | Al(OH)3 | Al2O3 |
| B | Na | Na2O2 | NaOH |
| C | H2SO3 | SO2 | H2SO4 |
| D | HCl | Cl2 | HClO |
| A. | A | B. | B | C. | C | D. | D |