题目内容
12.利用化学反应Fe+CuSO4═FeSO4+Cu设计原电池,下列有关描述正确的是( )| A. | Fe为正极 | B. | Cu为负极 | ||
| C. | 负极发生还原反应 | D. | 电解质溶液是CuSO4溶液 |
分析 根据Fe+CuSO4═FeSO4+Cu结合原电池原理知,铁作负极,铜作正极,负极上失电子发生氧化反应;正极上得电子发生还原反应.
解答 解:根据金属活动性顺序表知,铁比铜活泼,结合原电池原理知,铁作负极,铜作正极,负极上电极材料失电子变成离子进入溶液,发生氧化反应;正极上,溶液中铜离子得电子生成铜单质,反应还原反应,电解质溶液是CuSO4溶液;所以ABC错误,D正确,故选:D.
点评 原电池的设计思路:
1、根据反应方程式确定活泼性不同的两个电极;
2、根据反应方程式确定电解质溶液;
3、形成闭合回路;
4、能自发进行氧化还原反应.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
2.某10% NaOH溶液,加热蒸发掉100g水后得到80mL 20% 的溶液,则该20% NaOH溶液的物质的量浓度为
( )
( )
| A. | 5.25 mol/L | B. | 12.5 mol/L | C. | 7.5 mol/L | D. | 6.25 mol/L |
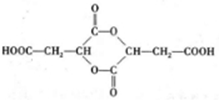
3.某种药物合成中间体的结构简式为: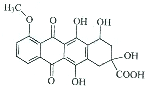 ,有关该物质的说法不正确的是( )
,有关该物质的说法不正确的是( )
 ,有关该物质的说法不正确的是( )
,有关该物质的说法不正确的是( )| A. | 属于芳香族化合物 | |
| B. | 能发生消去反应和酯化反应 | |
| C. | 能分别与金属Na、NaOH溶液反应 | |
| D. | 1mol该有机物与足量NaOH溶液反应,消耗5molNaOH |
20.下列有机实验操作或叙述正确的是( )
| A. | 甲烷和氯气在室温下的黑暗环境中不可以稳定存在 | |
| B. | 将乙烯和乙烷气体分别通入溴的四氯化碳溶液中前者褪色,后者不褪色 | |
| C. | 苯能使溴水褪色是因为二者反应生成了溴苯 | |
| D. | 要除去乙烷中的乙烯制得纯净的乙烷,可将混合气通入酸性高锰酸钾溶液中 |
7.下列试剂的贮存方法错误的是( )
| A. | 钠保存在煤油中 | |
| B. | 用带磨口玻璃塞的试剂瓶盛放NaOH溶液 | |
| C. | 存放液溴时需水封 | |
| D. | 保存氯化亚铁溶液时,要加入少量的铁粉 |
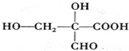
1.如图为某有机物的结构简式,该有机物不具有的性质是( )
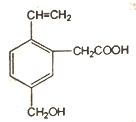

| A. | 能使酸性KMn04溶液褪色 | B. | 能发生酯化反应 | ||
| C. | 能与NaOH溶液反应 | D. | 能发生水解反应 |
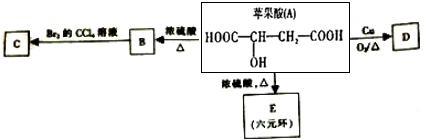
 .
. 、
、 (任一种).
(任一种).