题目内容
【题目】某校化学兴趣小组探究恒温(98℃)下乙酸乙酯制备实验中硫酸浓度对酯化反应的影响探究。实验得到数据如下表(各组实验反应时间均5分钟):
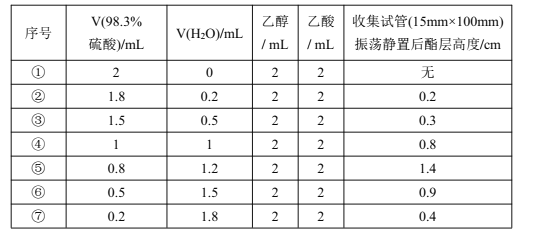
下列关于该实验的说法不正确的是
A.乙酸乙酯制备实验中起催化作用的可能是H+
B.浓硫酸的吸水作用、乙酸乙酯的蒸出均可以使酯化反应正向移动
C.浓硫酸和水以体积比约2∶3混合催化效果最好
D.⑤⑥⑦组可知c(H+)浓度越大,反应速率越慢
【答案】D
【解析】
乙酸乙酯的制备中,浓硫酸具有催化性、吸水性,并且乙酸和乙醇的酯化的可逆反应,浓硫酸吸水作用,乙酸乙酯的蒸出使平衡正向移动。
A. 从表中①可知,没有水,浓硫酸没有电离出H+,乙酸乙酯的收集为0,所以起催化作用的可能是H+,A项正确;
B. 浓硫酸的吸水作用、乙酸乙酯的蒸出均可以使酯化反应正向移动,B项正确;
C. 从表中⑤可知,浓硫酸和水以体积比约2∶3混合催化效果最好,C项正确;
D. 表中⑤⑥⑦组c(H+)浓度逐渐变小,收集的乙酸乙酯变小,反应速率越慢,D项错误。
答案选D。

练习册系列答案
 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目