题目内容
13.(1)某有机物的系统命名的名称为2,4-二甲基-3-乙基己烷,它的结构简式CH3CH(CH3)CH(CH2CH3)CH(CH3)CH2CH3,(2)按系统命名法给有机物
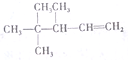 命名3,4,4-三甲基-1-戊烯
命名3,4,4-三甲基-1-戊烯(3)配制银氨溶液时,把氨水滴入硝酸银溶液的操作关键是直至生成的白色沉淀刚好溶解为止,乙醛与银氨溶液反应的化学方程式为CH3CHO+2Ag(NH3)2OH$\stackrel{水浴}{→}$CH3COONH4+2Ag↓+3NH3+H2O.
分析 (1)烷烃的命名原则:长、多、近、小、简,据此书写结构简式即可;
(2)烯烃的命名选取含有碳碳双键的最长碳链为主链,选取距离双键最近的一端为1号碳;
(3)氨水和硝酸银反应生成AgOH,AgOH继续与氨水反应生成银氨络离子;醛类可以发生银镜反应生成羧酸铵、金属单质银以及氨气.
解答 解:(1)2,4-二甲基-3-乙基己烷,主链6个C原子,2号碳和4号碳原子上各有1个甲基,3号碳原子有一个乙基,结构简式:CH3CH(CH3)CH(CH2CH3)CH(CH3)CH2CH3,故答案为:CH3CH(CH3)CH(CH2CH3)CH(CH3)CH2CH3,;
(2) 为戊烯,双键在1、2号碳之间,在3号碳和4号碳上分别含有1个和2个甲基,正确命名为:3,4,4-三甲基-1-戊烯,故答案为:3,4,4-三甲基-1-戊烯;
为戊烯,双键在1、2号碳之间,在3号碳和4号碳上分别含有1个和2个甲基,正确命名为:3,4,4-三甲基-1-戊烯,故答案为:3,4,4-三甲基-1-戊烯;
(3)配制银氨溶液时,将稀氨水慢慢滴加到稀硝酸银溶液中,产生白色沉淀后继续滴加到沉淀刚好溶解为止;乙醛可以发生银镜反应生成乙酸铵、金属单质银以及氨气,反应的化学方程式为:CH3CHO+2Ag(NH3)2OH$\stackrel{水浴}{→}$CH3COONH4+2Ag↓+3NH3+H2O,故答案为:直至生成的白色沉淀刚好溶解为止;CH3CHO+2Ag(NH3)2OH$\stackrel{水浴}{→}$CH3COONH4+2Ag↓+3NH3+H2O.
点评 本题主要考查的是烷烃结构简式书写、烯烃的命名和醛类的性质,难度不大,注意基础知识的掌握.

练习册系列答案
 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
3.用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 标准状况下,22.4L CCl4含有的分子数为NA | |
| B. | 2.4gMg溶于足量稀盐酸,转移的电子数为0.1NA | |
| C. | 通常状况下,32gO2与32gO3所含的氧原子数均为2NA | |
| D. | 质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 的数目为NA |
4.设NA为阿伏加德罗常数,下列叙述正确的是( )
| A. | 3.4gNH3中含有电子数为2NA | |
| B. | 0.1mol/L CuSO4溶液中含有的SO2-4数目为0.1NA | |
| C. | 常温常压下,2.24L O3中含有的氧原子数为0.3NA | |
| D. | 8.7gMnO2与50mL 8mol/L浓盐酸充分反应后,生成Cl2的氯分子数为0.1NA |
1.在酸性或碱性较强的溶液中,铝均可以溶解,但在家庭里,用食盐腌制的食品亦不能长期存放在铝制品中,其主要原因是( )
| A. | 铝能与NaCl直接发生反应而被氧化为氧化铝 | |
| B. | 长期存放的NaCl与水反应,溶液不再呈中性,可与铝发生反应 | |
| C. | 铝与其中的杂质、NaCl溶液形成原电池,铝被氧化 | |
| D. | 铝与其中的杂质、NaCl溶液形成原电池,铝被还原 |
18.烃类分子中的碳原子与其它原子的结合方式是( )
| A. | 形成四对共用电子对 | B. | 通过非极性键 | ||
| C. | 通过两个共价键 | D. | 通过离子键和共价键 |
2.若20g密度为ρ g•cm-3的Ca(NO3)2溶液中含有2g Ca(NO3)2,则溶液中NO3-的物质的量浓度为( )
| A. | $\frac{ρ}{400}$mol•L-1 | B. | $\frac{20}{ρ}$mol•L-1 | C. | $\frac{50ρ}{41}$mol•L-1 | D. | $\frac{25ρ}{41}$mol•L-1 |
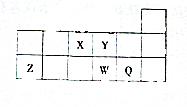 短周期元素X、Y、Z、W、Q在元素周期表中相对位置如图所示
短周期元素X、Y、Z、W、Q在元素周期表中相对位置如图所示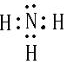 ,其水溶液呈碱性性(填酸、碱或中)
,其水溶液呈碱性性(填酸、碱或中)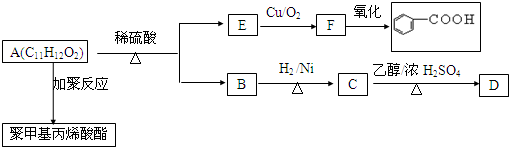
 .
.