题目内容
【题目】化学实验装置的科学设计是实验是否取得预期效果的关键。请回答下列有关实验装置的相关问题:

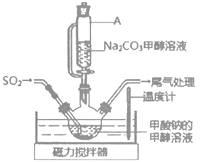
I.图一中A为教材制备乙酸乙酯的实验装置,甲同学认为图一中B装置比A要好,则冷却水应从______口进入;乙同学认为图一中C装置效果更好,理由是_______。
Ⅱ.“摩尔盐”[(NH4)2Fe(SO4)26H2O]是分析化学中的重要试剂。已知:摩尔盐隔绝空气加热至500℃时可完全分解。某学习小组欲探究其分解产物。
(1)[提出猜想]小组同学认为分解产物可能有以下几种情况:
A.Fe2O3、SO2、NH3、H2O B.FeO、SO3、NH3、H2O
C.FeO、SO2、NH3、H2O D.Fe2O3、SO3、SO2、NH3、H2O
根据所学知识,可确定_________不成立(填序号)
(2)[药品验纯]甲同学提出可以用湿润的红色石蕊试纸、稀盐酸和_________溶液检验出“摩尔盐”中的三种离子;取一定量的“摩尔盐”配成溶液,取少量溶液置于试管中,向其中滴加_______(填试剂名称和实验现象),则“摩尔盐”未因氧化而变质。
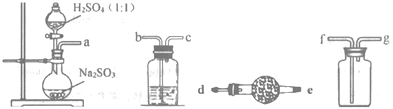
(3)[实验探究]为检验分解产物,甲同学设计了如下实验装置。
①取一定量“摩尔盐”置于加热管A中,加热至分解完全后打开K,再通入N2,目的是________。
②实验中观察到A中固体逐渐变为红棕色,B、C中均产生白色沉淀.C中发生反应的离子方程式为________。
③实验验证取A中残留物少许加入稀硫酸溶解,再滴入KMnO4稀溶液,不褪色证明产物不含______。
(4)[实验结论与反思]通过实验现象和认真反思,上述猜想中一定正确的是______。(填序号)
【答案】b 既能冷凝回流又能及时分离出反应生成的水,有利于酯的生成 C Ba(OH)2 硫氰化钾溶液,溶液不变红色 使分解产生的气体在B、C中被吸收充分 SO2+H2O2+Ba2+=BaSO4↓+2H+ FeO A
【解析】
I.为充分冷凝蒸气,冷却水的流向和蒸气的流向应该相反,所以冷却水应从b口进入;C装置既能冷凝回流又能及时分离出反应生成的水,有利于酯的生成。故答案为b,既能冷凝回流又能及时分离出反应生成的水,有利于酯的生成。
Ⅱ.(1)A. “摩尔盐”中铁的化合价为+2价,硫为+6价,生成物中铁为+3价,硫为+4价,化合价既有升高又有降低,所以A合理;
B.没有任何一种元素的化合价发生变化,所以B合理;
C.只有硫的化合价降低,不符合氧化还原反应的要求,所以C不合理;
D.铁的化合价升高,硫的化合价部分降低,所以D合理。
所以选C。
(2)“摩尔盐”中含有NH4+,可以加入强碱溶液,加热,用湿润的红色石蕊试纸检验逸出的氨气。加入强碱溶液后,Fe2+可以和OH-生成Fe(OH)2白色沉淀,白色沉淀会迅速变成灰绿色,最后变成红褐色的Fe(OH)3,可以据此检验Fe2+。SO42-可以用稀盐酸和Ba2+检验,产生不溶于盐酸的白色沉淀BaSO4,所以选择既可以提供OH-又能提供Ba2+的Ba(OH)2溶液;若“摩尔盐”因氧化而变质,则会存在Fe3+,可以用KSCN溶液检验。故答案为Ba(OH)2,硫氰化钾溶液,溶液不变红色。
(3)①“摩尔盐”加热分解完全后打开K,再通入N2,目的是使分解产生的气体在B、C中被吸收充分。
②实验中观察到C中产生白色沉淀,原因是SO2通入C中,被H2O2氧化为SO42-,SO42-和Ba2+生成了BaSO4。则C中发生反应的离子方程式为SO2+H2O2+Ba2+=BaSO4↓+2H+。
③A中残留物少许加入稀硫酸溶解,再滴入KMnO4稀溶液,若产物中有FeO,则溶于稀硫酸后生成的Fe2+能使KMnO4稀溶液褪色,KMnO4稀溶液不褪色证明产物不含FeO。
(4)实验中观察到A中固体逐渐变为红棕色,所以“摩尔盐”分解产生了Fe2O3,B中产生白色沉淀,可能是生成了SO3,进入水溶液中后和水反应生成了H2SO4,H2SO4和BaCl2反应生成了BaSO4,也可能是氨气和SO2一起进入B中,氨和SO2生成的(NH4)2SO3和BaCl2反应生成了BaSO3。C中产生白色沉淀,是SO2通入C中,被H2O2氧化为SO42-,SO42-和Ba2+生成了BaSO4。所以一定有SO2和Fe2O3生成。则上述猜想中一定正确的是A。

【题目】实验室可利用环己醇的氧化反应制备环己酮,反应原理和实验装置(部分夹持装置略)如下:

有关物质的物理性质见下表。
物质 | 沸点(℃) | 密度(g·cm-3,20℃) | 溶解性 |
环己醇 | 161.1(97.8)* | 0.96 | 能溶于水和醚 |
环己酮 | 155.6(95.0)* | 0.95 | 微溶于水,能溶于醚 |
水 | 100.0 | 1.0 |
*括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点。
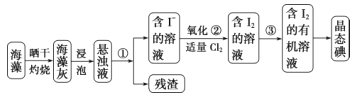
实验中通过装置B将酸性Na2Cr2O7溶液加到盛有10 mL环己醇的A中,在55 ~ 60℃进行反应。反应完成后,加入适量水,蒸馏,收集95 ~ 100℃的馏分,得到主要含环己酮粗品和水的混合物。
(1)装置D的名称为____________________________。
(2)酸性Na2Cr2O7溶液氧化环己醇反应的![]() ,反应剧烈将导致体系温度迅速上升,副反应增多。
,反应剧烈将导致体系温度迅速上升,副反应增多。
①滴加酸性Na2Cr2O7溶液的操作为____________________________________________;
②蒸馏不能分离环己酮和水的原因是__________________________________________。
(3)环己酮的提纯需要经过以下一系列的操作:
a.蒸馏、除去乙醚后,收集151~156℃馏分
b.水层用乙醚(乙醚沸点34.6℃,易燃烧)萃取,萃取液并入有机层
c.过滤
d.往液体中加入NaCl固体至饱和,静置,分液
e.加人无水MgSO4固体,除去有机物中少量的水
①上述提纯步骤的正确顺序是________________________________________________;
②B中水层用乙醚萃取的目的是______________________________________________;
③上述操作c、d中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需要的玻璃仪器有__________,操作d中,加入NaC1固体的作用是_____________________________。
(4)恢复至室温时,分离得到纯产品体积为6 mL,则环已酮的产率为____________。(计算结果精确到0.1%)