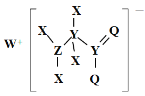题目内容
【题目】短周期主族元素 A、B、C、D、E 的原子序数依次增大。常温下,A、C 组成的化合物是常见液体,B 原子最外层电子数等于次外层电子数的 2 倍,D 与 C 同主族。回答下列问题:
(1) A 的单质的电子式为 ______ ;B 在元素周期表中的位置为第____周期第_____ 族。
(2) B、C 中,原子半径大的是______(填元素符号);D、E 的简单氢化物中,稳定性较强的是______(填化学式)。
(3) A、C 组成的原子个数比为 1:1 的化合物常用于制备 C 的单质,反应的化学方程式为 _______ 。
【答案】H∶H 二 ⅣA C HCl 2H2O2 ![]() 2 2H2O2+O2↑
2 2H2O2+O2↑
【解析】
常见的无色液体是水,因此,A是氢元素,C是氧元素。B应该位于第二周期,B原子最外层电子数等于次外层电子数2倍,则B是碳元素。D与氧元素同主族,则D是硫元素,E只能是氯元素。
(1)H2的电子式为H∶H;碳原子的电子层数为2,最外层电子数为4,它位于第二周期、ⅣA族,
故答案为:H∶H ;二 ;ⅣA;
(2)同一周期从左到右,元素的原子半径依次减小,所以,铍与氧中,原子半径较大的是C;同一周期从左到右,元素的非金属性依次增强,所以,非金属性:Cl>S,两种元素的简单氢化物中稳定性较强的是HCl,
故答案为:C ; HCl;
(3)氢元素与氧元素可组成两种化合物,其中原子个数比为1:1的化合物是H2O2,实验室常用过氧化氢的分子反应制备氧气,反应的化学方程式为:2H2O2 ![]() 2 2H2O2+O2↑,
2 2H2O2+O2↑,
故答案为:2H2O2 ![]() 2 2H2O2+O2↑。
2 2H2O2+O2↑。

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目