��Ŀ����
����Ŀ����������茶���[��NH4��2Fe��SO4��2��6H2O]�Ƿ�����ѧ����Ҫ���Լ��������ڴ���������������������茶�����500��Cʱ��������������ȫ�ֽ⡣�ش��������⣺
��1����������茶����������������ȫ�ֽ⣬������������ԭ��Ӧ��������������FeO��Fe2O3��������������NH3��SO3��H2O��N2��__________________
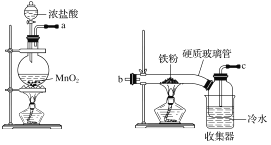
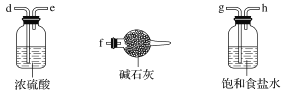
��2��Ϊ����ֽ����ijɷ֣��������ʵ��װ�ý���ʵ�飬����A�е���������茶������ֽ���ȫ��

��A�й����ּ��Ƚϳ�ʱ���ͨ�뵪����Ŀ����_______________________________��
��Ϊ����A�в������Ƿ���FeO����Ҫѡ�õ��Լ���______________�����ţ���
A.KSCN��Һ B.ϡ���� C.Ũ���� D.KMnO4��Һ
��3��ͨ�����Ը��������Һ����Һ��ɫ���÷�Ӧ��SO2���ֳ���ѧ������_____
���𰸡�SO2 ʹ�ֽ������������B��C�б����ճ�� BD ��ԭ��
��������
��1����Ԫ�غ���Ԫ�ػ��ϼ�����,������������ԭ��Ӧ�л��ϼ��������н�,���ϼ۽��͵�Ӧ������,������������л�������SO2;
��2����A�й����ּ��Ƚϳ�ʱ���,ͨ�뵪��Ŀ����ʹ�ֽ����ɵ�������B��Cװ������ȫ���գ�
��Ϊ��֤A�в������Ƿ���FeO��Ӧ������ϡ�����ܽ�,Ȼ������KMnO4��Һ������������,����BDѡ������ȷ��,
��3��ͨ�����Ը��������Һ����Һ��ɫ�����������������÷�Ӧ��SO2���ֳ��Ļ�ѧ�����ǻ�ԭ�ԡ�

����Ŀ����֪Ksp(CaCO3)=2.8��10-9�������й���Ϣ:
���� | CH3COOH | H2CO3 |
����ƽ�ⳣ��(����) | Ka=1.8��10-5 | Ka1=4.3��10-7�� Ka2=5.6��10-11 |
�����ж���ȷ����
A. ��Na2CO3��Һ�е����̪,��Һ��죬��Ҫԭ����CO32��+2H2O![]() H2CO3+2OH��
H2CO3+2OH��
B. ����ʱ��CH3COOH��CH3COONa�����Һ��pH=6����c(CH3COOH)/c(CH3COO-)��18
C. NaHCO3��Һ��:c(OH-)-c(H+)=c(H2CO3)-c(CO32��)
D. 2��10-4 mol/L��Na2CO3��Һ��CaCl2��Һ�������ϳ��ֳ�������CaCl2��Һ��Ũ��һ����5.6��10-5 mol/L
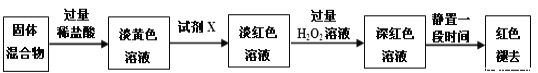
����Ŀ������DZȽ���Ҫ���������ʣ���ش��������⣺
��1���Ȼ����Һ������ϴ���������⼣��д����ط�Ӧ�����ӷ���ʽ��_________________
��2��ʵ�����������þ�������Ȼ����Һ�У������۵㣺�Ȼ��ˮ���������к�OH-��ʹ������þ�����ܽ�ƽ�����ƣ�笠����OH-��ʹ������þ�����ܽ�ƽ�����ơ�Ϊ��̽����Ӧ������������Һ�м���_____����Һ��֤��
��3��NH4SCN��Һ��AgNO3��Һ��Ӧ������ AgSCN��������֪�������£�Ksp(AgCl)=1.8��10��10,Ksp(AgSCN)= 2.0��10��12����AgClת��ΪAgSCN��ƽ�ⳣ��K=____________
��4����������100mL0.2mo/L�İ�ˮ����μ���0.2mol/L�����ᣬ������Һ��pH����Һ��NH4+��NH3��H2O���ʵ���������������������Ĺ�ϵ����ͼ��ʾ������ͼ��ش��������⡣

�ٱ�ʾNH3��H2OŨ�ȱ仯��������__________(�A����B")��
��NH3��H2O�ĵ��볣��Ϊ__________________(��֪lg1.8 = 0.26)��
�۵������������Ϊ50mLʱ����Һ��c(NH4+)��c(NH3��H2O) =_____mol/L (�����ֱ�ʾ)��
��5��Ϊ��̽������������Ȼ��ˮ��ƽ���Ӱ�죬�������ʵ�鷽����
ʵ����� | c��NH4Cl��/mol��L-1 | �¶�/�� | ���������� | ʵ��Ŀ�� |
�� | 0.5 | 30 | x | - |
�� | 1.5 | i | y | ̽��Ũ�ȶ��Ȼ��ˮ��ƽ���Ӱ�� |
�� | 0.5 | 35 | z | ii |
�� | 2.0 | 40 | m | ̽���¶ȡ�Ũ��ͬʱ���Ȼ��ˮ��ƽ���Ӱ�� |
��ѡҩƷ������������ˮԡ��pH�ơ��ձ���0.1mol��L-1��������Һ������ˮ����Ũ�ȵ�NH4Cl��Һ��
��ʵ���У�����������������_______________
��i=____________________��ii��___________________________________
������������y____���������������=����m��