题目内容
8. 如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cs+离子核间距为a cm,氯化铯的摩尔质量为M,NA为阿伏加德罗常数,则氯化铯晶体的密度为( )
如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cs+离子核间距为a cm,氯化铯的摩尔质量为M,NA为阿伏加德罗常数,则氯化铯晶体的密度为( )| A. | $\frac{8M}{{N}_{A}•{a}^{3}}$g.cm-3 | B. | $\frac{M{a}^{3}}{8{N}_{A}}$gcm-3 | C. | $\frac{M}{{N}_{A}•{a}^{3}}$g.cm-3 | D. | $\frac{Ma}{{N}_{A}}$g.cm |
分析 晶体中2个最近的Cs+核间距为acm,相邻顶点上Cs+核间距离最近,为acm,即晶胞的棱长为acm,体积V=a3cm3,该晶胞中Cs+个数=8×$\frac{1}{8}$=1,Cl-个数为1,根据晶胞密度公式ρ=$\frac{m}{V}$计算氯化铯密度.
解答 解:氯离子位于顶点,晶胞中数目为8×$\frac{1}{8}$=1,铯离子位于体心,数目为1,即一个晶胞中含有一个氯离子和一个铯离子,则一个晶胞质量为 $\frac{M}{N{\;}_{A}}$g,2个最近的Cs+离子核间距为acm,即晶胞边长为acm,则晶胞体积为a3cm3,则密度为 $\frac{M}{{N}_{A}•{a}^{3}}$g•cm-3,
故选C.
点评 本题考查晶胞密度计算,难度不大,应准确计算出晶胞所含微粒数目.

练习册系列答案
相关题目
18.下列说法不正确的是( )
| A. | 同族元素,随着电子层的增加,I1逐渐增大 | |
| B. | 通常情况下,电离能I1<I2<I3 | |
| C. | 同周期元素,随着核电荷数的增加,I1呈增大趋势 | |
| D. | 电离能越小,元素的金属性越强 |
3. 绿茶中含有物质EGCG具有抗癌作用,能使癌细胞自杀性死亡其结构见图.下列有关EGCG的说法中正确的是( )
绿茶中含有物质EGCG具有抗癌作用,能使癌细胞自杀性死亡其结构见图.下列有关EGCG的说法中正确的是( )
 绿茶中含有物质EGCG具有抗癌作用,能使癌细胞自杀性死亡其结构见图.下列有关EGCG的说法中正确的是( )
绿茶中含有物质EGCG具有抗癌作用,能使癌细胞自杀性死亡其结构见图.下列有关EGCG的说法中正确的是( )| A. | EGCG易被氧化 | |
| B. | EGCG的分子中有1个手性碳原子 | |
| C. | 1mol EGCG与浓溴水发生取代反应时最多消耗6molBr2 | |
| D. | 1mol EGCG与氢氧化钠溶液反应最多消耗10molNaOH |
13.某短周期非金属元素的原子核外最外层电子数是次外层电子数的一半,该元素( )
| A. | 单质常用作半导体材料和光导纤 | B. | 在自然界中以化合态的形式存在 | ||
| C. | 最高价氧化物不与任何酸反应 | D. | 气态氢化物比甲烷稳定 |
20.将2mol SO2和1mol O2充入一容积固定的密闭容器中,在一定条件下反应:2SO2(g)+O2(g)?2SO3(g),下列哪些情况能说明化学反应已达反应限度的是( )
| A. | 每生成2mol SO2的同时,消耗2molSO3 | |
| B. | 混合气体的总质量不再变化 | |
| C. | 每生成2mol SO3的同时,消耗1molSO2 | |
| D. | 混合气体的压强不再变化 |
20.将甲苯与液溴混合,加入铁粉,其反应所得的产物可能有( )
①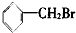 ②
②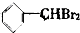 ③
③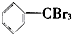 ④
④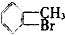 ⑤
⑤ ⑥
⑥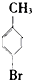 ⑦
⑦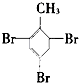
①
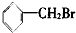 ②
②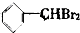 ③
③ ④
④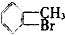 ⑤
⑤ ⑥
⑥ ⑦
⑦
| A. | 仅①②③ | B. | 仅⑦ | C. | 仅④⑤⑥⑦ | D. | 全部 |
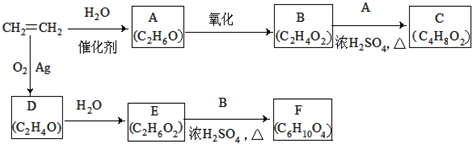
 .
.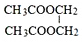 .
.