题目内容
7.市售浓H2SO4中,溶质的质量分数为98%,密度为1.984g•cm3.计算市售浓H2SO4中,H2SO4的物质的量浓度.分析 溶质质量分数与物质的量浓度的关系为:c=$\frac{1000ρω}{M}$,据此可计算出该硫酸的物质的量浓度.
解答 解:溶质的质量分数为98%,密度为1.984g•cm3的浓H2SO4的物质的量浓度为:c(H2SO4)=$\frac{1000×1.984×98%}{98}$mol/L=19.84mol/L,
答:该浓硫酸的物质的量浓度为19.84mol/L.
点评 本题考查了物质的量浓度的计算,题目难度不大,明确物质的量浓度与溶质质量分数的转化关系为解答关键,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.电子层数相同的三种元素X、Y、Z,它们最高价氧化物对应水化物的酸性由强到弱顺序为:HXO4>H2YO4>H3ZO4,下列判断不正确的是( )
| A. | 原子半径X>Y>Z | |
| B. | 气态氢化物稳定性X>Y>Z | |
| C. | 元素原子得电子能力由强到弱X>Y>Z | |
| D. | 单质与氢气反应由易到难X>Y>Z |
2.氢气是未来理想的能源,用MnFe2O4热化学循环制氢气的原理如下(x不为零):MnFe2O4→MnFe2O4-x(s)+$\frac{x}{2}$O2(g)△H1;MnFe2O4-x(s)+xH2O(g)═MnFe2O4(s)+xH2(g)△H2,下面说法正确的是( )
| A. | 上述两个反应都是氧化还原反应,且转移电子数相等 | |
| B. | Mn与Fe都属于ⅤⅡ族元素 | |
| C. | 2H2(g)+O2(g)=2H2O(g)△H=-2(△H1+△H2) | |
| D. | 根据两个反应可以看出,非自发反应加入合适的催化剂可以自发进行 |
1.一定条件下存在反应:CO(g)+H2O(g)?CO2(g)+H2(g)△H=-QkJ/mol.现有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在 I中充入1molCO和1molH2O,在Ⅱ中充入1molCO2和1mol H2,在Ⅲ中充入2molCO和2molH2O,700℃条件下开始反应.达到平衡时,上述三个过程对应的能量变化值分别为Q1、Q2、Q3.下列说法正确的是( )
| A. | 2Q1=2Q2<Q3 | |
| B. | 容器Ⅰ中CO的百分含量比容器Ⅲ中CO的百分含量高 | |
| C. | 容器Ⅰ中反应的平衡常数比容器Ⅱ中反应的平衡常数小 | |
| D. | 容器Ⅰ中CO的转化率与容器Ⅱ中CO2的转化率之和等于1 |
19.霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物,它在酸性溶液中能发生如下反应:
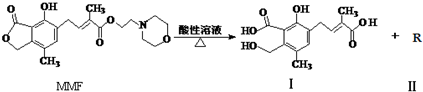
下列说法中正确的是( )

下列说法中正确的是( )
| A. | 1molMMF与足量NaOH 溶液共热,最多可消耗5molNaOH | |
| B. | 可以用NaHCO3溶液区别MMF与化合物Ⅰ | |
| C. | 化合物 R的分子式为C6H13NO2 | |
| D. | 一个MMF分子中含有2个手性碳原子 |


 ,其中心原子的杂化类型是sp3杂化
,其中心原子的杂化类型是sp3杂化 .
. 2001年诺贝尔化学奖被美国的诺尔斯、夏普雷斯和日本的野依良治获得,他们发现了某些手性化子可用作某些化学反应的催化剂,为合成对人类有用的重要化合物开辟了一个全新的研究领域.
2001年诺贝尔化学奖被美国的诺尔斯、夏普雷斯和日本的野依良治获得,他们发现了某些手性化子可用作某些化学反应的催化剂,为合成对人类有用的重要化合物开辟了一个全新的研究领域. 、
、 .
. ②
② ③
③
 .
.