题目内容
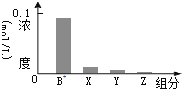
【题目】室温下,![]() 的一元碱BOH与等浓度的盐酸等体积混合后,所得溶液中部分微粒的组分及浓度如图所示,下列对混合溶液的分析正确的是( )
的一元碱BOH与等浓度的盐酸等体积混合后,所得溶液中部分微粒的组分及浓度如图所示,下列对混合溶液的分析正确的是( )
A.溶液显中性B.升温,![]() 增大,
增大,![]() 减小
减小
C.![]() D.稀释溶液,
D.稀释溶液,![]() 增大,
增大,![]() 增大
增大
【答案】C
【解析】
![]() 的一元碱BOH与等浓度的盐酸等体积混合后,
的一元碱BOH与等浓度的盐酸等体积混合后,![]() ,所得溶液中
,所得溶液中![]() 浓度小于
浓度小于![]() ,说明在溶液中存在
,说明在溶液中存在![]() ,BOH为弱碱,BCl溶液呈酸性,则
,BOH为弱碱,BCl溶液呈酸性,则![]() ,一般来说,盐类的水解程度较小,则:
,一般来说,盐类的水解程度较小,则:![]() ,反应后溶液中离子浓度大小为:
,反应后溶液中离子浓度大小为:![]() 即X表示
即X表示![]() ,Y表示BOH,Z表示
,Y表示BOH,Z表示![]() ,溶液中存在物料守恒为:
,溶液中存在物料守恒为:![]() ,据此解答。
,据此解答。
![]() 的一元碱BOH与等浓度的盐酸等体积混合后,
的一元碱BOH与等浓度的盐酸等体积混合后,![]() ,所得溶液中
,所得溶液中![]() 浓度小于
浓度小于![]() ,说明在溶液中存在
,说明在溶液中存在![]() ,BOH为弱碱,BCl溶液呈酸性,则
,BOH为弱碱,BCl溶液呈酸性,则![]() ,一般来说,盐类的水解程度较小,则:
,一般来说,盐类的水解程度较小,则:![]() ,反应后溶液中离子浓度大小为:
,反应后溶液中离子浓度大小为:![]() 即X表示
即X表示![]() ,Y表示BOH,Z表示
,Y表示BOH,Z表示![]() ,溶液中存在物料守恒为:
,溶液中存在物料守恒为:![]() ,
,
A.BOH为弱碱,反应生成强酸弱碱盐BCl,则溶液显酸性,故A错误;
B.盐的水解为吸热反应,升温促进水解,则Y浓度增大,故B错误;
C.X表示![]() ,Y表示BOH,Z表示
,Y表示BOH,Z表示![]() ,溶液中存在物料守恒为:
,溶液中存在物料守恒为:![]() ,故C正确;
,故C正确;
D.稀释后促进水解,但是溶液中氢离子浓度减小,即![]() 减小,故D错误;
减小,故D错误;
故答案选C。

练习册系列答案
 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目