题目内容
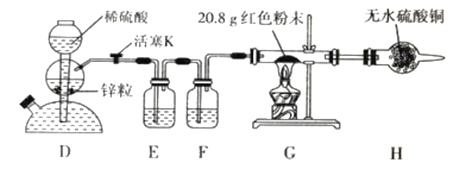
【题目】某学习小组利用下图装置(夹持装置略去)测定某铁硫化物(FexSy)的组成。
[实验步骤]
(1)组装仪器:上述四个装置的正确连接顺序为____;
(2)检査装置气密性:应如何操作?____;
(3)加入药品,开始实验:应先____,一段时间后再____;
(4)停止反应:当硬质玻璃管中固体质量不再改变时,停止加热,继续通入—段时间的O2,其目的是____;
(5)测定S元素的质量:将B中所得溶液加水配制成250 mL溶液,取25.00 mL所配溶液,加入足量的双氧水,再加入足量盐酸酸化的BaCl2溶液,将所得沉淀过滤、洗涤、干燥,称其质量为2.33g。之前所取铁硫化物得质量为6g,则FexSy的化学式为____;
[实验反思与再探究]
(6)有同学认为步骤(5)可以设计为:取25.00 mL所配溶液,加入足量的BaCl2溶液,将所得沉淀过滤、洗涤、干燥,称得BaSO3沉淀的质量。你认为此方案____(填“是”或“否”)合理,理由是____。
(7)有同学为了继续探究反应后硬质玻璃管中固体的成分,他将固体取出,完全溶于稀硫酸中,再向溶液中加入K3Fe(CN)6溶液,未观察到明显现象,则硬质玻璃管中所发生反应的化学方程式为____。
【答案】 ADCB (用带止水夹的胶管)封住B的出气口,(保证分液漏斗不断水的情况下)从分液漏斗向烧瓶加水;若某时水不再流下,则装置的气密性良好 打开分液漏斗旋塞(或制氧气) 点燃酒精喷灯(或加热) 使生成的SO2全部被NaOH溶液吸收 FeS2 否 SO32— (或答为Na2 SO3、Ba SO3)可能被氧化 4FeS2 + 11O2![]() 2Fe2O3 + 8SO2
2Fe2O3 + 8SO2
【解析】该实验的目的是测定某铁硫化物(FexSy)的组成。观察所给装置,A为产生氧气的装置,氧气进入C与铁硫化物反应生成二氧化硫,B的作用即为吸收二氧化硫,计算硫的质量,得出铁硫化物(FexSy)的组成。
(1)氧气进入C前先除去水蒸气,再与铁硫化物反应生成二氧化硫,通过计算硫的质量,得出铁硫化物(FexSy)的组成。上述四个装置的正确连接顺序为ADCB;
(2)检查装置的气密性则需要封住B的出气口,(保证分液漏斗不断水的情况下)从分液漏斗向烧瓶加水;若某时水不再流下,则装置的气密性良好;
(3)加入药品,开始实验:应先打开分液漏斗的活塞,使氧气充满整个妆之后再点燃酒精喷灯,开始反应;
(4)因为本实验的关键是准确测的硫的质量。故停止反应:当硬质玻璃管中固体质量不再改变时,停止加热,继续通入—段时间的O2,其目的是使生成的SO2全部被NaOH溶液吸收;
(5)将B中所得溶液加水配制成250 mL溶液,取25.00 mL所配溶液(取了十分之一溶液),加入足量的双氧水,将亚硫酸钠氧化到硫酸钠,再加入足量盐酸酸化的BaCl2溶液,所得沉淀为BaSO4,为2.33g,0.01mol。故250 mL溶液中n(S)=0.1mol,6g铁硫化物中S的质量为3.2g,则Fe的质量为2.8g,0.05mol,故x:y=1:2,则FexSy的化学式为FeS2;
(6)若取25.00 mL所配溶液,加入足量的BaCl2溶液,称BaSO3沉淀的质量,不合理,因为Ba SO3在空气中会被氧化成BaSO4;
(7)将固体完全溶于稀硫酸中,再向溶液中加入K3Fe(CN)6溶液,未观察到明显现象,则说明溶液中没有Fe2+,则铁应被氧化成+3,为Fe2O3,故硬质玻璃管中所发生反应的化学方程式为4FeS2 + 11O2![]() 2Fe2O3 + 8SO2。
2Fe2O3 + 8SO2。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案【题目】CO2是引起“温室效应”的主要物质,CO2的甲烷化可以实现其循环利用。
甲烷化过程中,可能发生如下反应:
I. CO2 (g)+4H2(g) ![]() CH4(g)+2H2O(g) △H1
CH4(g)+2H2O(g) △H1
II. CO2 (g)+4H2(g) ![]() CO(g)+2H2O(g) △H2
CO(g)+2H2O(g) △H2
已知反应II中相关的化学键键能数据如下:
化学键 | H—H | C=O | C | H—O |
E/(kJ·mol-1) | 436 | 750 | 1076 | 463 |
由此计算△H2=_________________。
(2)在常压、催化剂条件下,将CO2 和H2 (体积比为1:4,总物质的量为m mol)置于密闭容器中,发生反应I和II。测得CO2转化率、CH4和CO选择性随温度变化情况分别如图1和图2所示(选择性:转化的CO2中生成CH4或CO的百分比)

①由图1和图2可知,△H1___0(填“>”或“<”),____________可影响催化剂的选择性。
②由图1可知CO2的转化率呈现先升高后降低的变化趋势,其原因是________________________________。
③下列措施能提高CO2平衡转化率的是__________(填标号)
A.提高原料气中H2所占比例 B.适当增大压强 C.升高温度 D.增大催化剂的比表面积 E.前段加热,后段冷却
④350℃时,反应在t1时刻达到平衡,平衡时容器体积为VL,该温度下反应I的平衡常数为_____(用m、V表示)。
⑤550℃时,反应在t2时刻达到平衡,此时容器中H2O(g)的物质的量为__mol(用m表示)
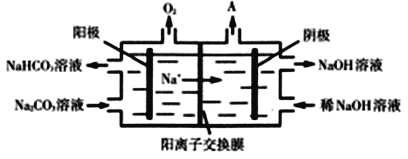
(3)CO2与NaOH溶液反应得到Na2CO3溶液。电解Na2CO3溶液的原理如图所示,阳极的电极反应式为______________________________________。
【题目】含氮化合物在工农业生产中都有重要应用。
(1)肼(N2H4)与亚硝酸反应可生成氮的另一种氢化物,在标准状况下,该氢化物气体的密度为1.92g/L,且其中氮元素的质量分数为0.977,则该反应的化学方程式为____.
(2)二氧化氮在一定条件下,可以发生如下反应:SO2(g)+NO2(g)![]() SO3(g)+NO(g) △H= -42kJ·mol-1,在2L的恒容密闭容器中充入SO2(g)和NO2(g)所得实验数据如下:
SO3(g)+NO(g) △H= -42kJ·mol-1,在2L的恒容密闭容器中充入SO2(g)和NO2(g)所得实验数据如下:
实验编号 | 温度 | 起始物质的量mol | 平衡时物质的量/mol | |
n(SO2) | n(NO2) | n(NO) | ||
甲 | T1 | 4.0 | 1.0 | 0.9 |
乙 | T2 | 1.0 | 4.0 | 0.8 |
丙 | T2 | 0.4 | 0.6 | a |
①在实验甲中,若2min时测得放出的热量是8.4kJ,0~2min时间内,用SO2表示的平均反应速率v(SO2)=_______________,该温度下的平衡常数为_________。(结果保留到小数点后两位)
②由表中数据可推知:T1_______T2(填“>”“<”或“=”)
③实验丙中,达到平衡时NO2的转化率为______________.
(3)工业上可以用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4。室温下测得NH4HSO3溶液pH为6,则溶液的![]() ________________________.(已知:H2SO3的Kal =1.5×10-2Ka2 =1.0×10-7)
________________________.(已知:H2SO3的Kal =1.5×10-2Ka2 =1.0×10-7)
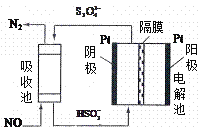
(4)使用间接电化学法可以处理煤烟气中的NO,装置如图,已知电解池溶液的pH在4~7之间,写出阴极的电极反应式__________________。
 。
。