题目内容
13.(1)“西气东输”中的“气”指天然气,其主要成分的化学式是CH4,一定量的该气体燃烧过程的能量变化如图1所示,从图中可以读出E1>E2(填“>”或“<”),该反应放出(填“放出”或“吸收”)能量.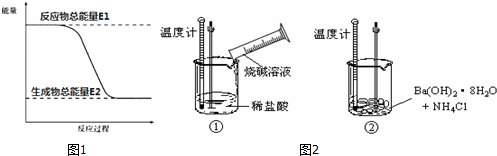
(2)某同学进行如图2的实验,探究化学反应中的能量变化.通过实验测出,反应前后①烧杯中的温度升高,②烧杯中的温度降低.由此判断Ba(OH)2•8H2O跟NH4Cl的反应是吸热(填“吸热”或“放热”)反应.试写出Ba(OH)2•8H2O与NH4Cl反应的化学反应方程式Ba(OH)2•8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O.
分析 (1)根据天然气的其主要成分为甲烷,化学式CH4;根据图可知反应物的总能量大于生成物的总能量;根据反应物所具有的总能量高于生成的总能量,为放热反应,反之为吸热反应;
(2)根据温度升高,反应放热,温度降低、反应吸热;根据铵盐与碱反应的规律写出化学方程式.
解答 解:天然气的其主要成分为甲烷,化学式CH4,由图可知反应物的总能量大于生成物的总能量,由反应物所具有的总能量高于生成的总能量,在反应中会有一部分能量转变为热能的形式释放,为放热反应,
故答案为:CH4;>;放出.
(2)②烧杯中的温度降低,所以Ba(OH)2•8H2O跟NH4Cl的反应是吸热反应,Ba(OH)2•8H2O跟NH4Cl反应是复分解反应,方程式为:Ba(OH)2•8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O;
故答案为:吸热;Ba(OH)2•8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O;
点评 本题主要考查了化学反应中能量变化,根据实验现象判断放热与吸热反应,难度不大,根据课本即可完成.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
3.下列叙述与蛋白质或糖类物质性质有关,并正确的是( )
| A. | 苯酚溶液不慎沾到皮肤上,立即用酒精溶液洗涤 | |
| B. | 任何条件下,稻草不可能转变为葡萄糖或酒精 | |
| C. | 氯化汞(HgCl2)的稀溶液不可用于手术器械消毒,因为它会使人体蛋白质变性 | |
| D. | 浓HNO3溅在皮肤上,使皮肤呈黄色,是由于浓HNO3和蛋白质发生颜色反应 |
4.在常温常压下,等物质的量的下列物质完全燃烧,消耗氧气最多的是( )
| A. | 甲烷 | B. | 乙醇 | C. | 苯 | D. | 乙酸乙酯 |
8.物质的量浓度都是0.1mol/L的CH3COOH和CH3COONa混合溶液,已知其中c(CH3COO-)>c(Na+),对该溶液的下列判断正确的是( )
| A. | c(H+)<c(OH-) | B. | c(CH3COOH)+c(CH3COO-)=0.2mol/L | ||
| C. | c(CH3COOH)>c(CH3COO-) | D. | c(CH3COO-)+c(OH-)=0.1mol/L |
18.日本福岛核电站事故发生后,在广东产蔬菜中检测到的极微量放射性${\;}_{53}^{131}$I,对公众健康没有影响,无需采取防护措施,公众不必担心.下列对该粒子的说法不正确的是( )
| A. | 质量数131 | B. | 核外电子数131 | C. | 原子序数53 | D. | 核内有78个中子 |
5.下列叙述正确的是( )
| A. | 除去乙烷中少量的乙烯:通过KMnO4溶液,再用浓硫酸干燥 | |
| B. | 除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤,分液 | |
| C. | 鉴别溴乙烷中的溴原子,可直接加入AgNO3溶液 | |
| D. | 除去乙醇中少量的水:加足量生石灰,蒸馏 |
2.有一种有机物结构简式为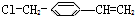 推测它不可能具有下列哪种性质( )
推测它不可能具有下列哪种性质( )
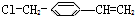 推测它不可能具有下列哪种性质( )
推测它不可能具有下列哪种性质( )| A. | 能被酸性高锰酸钾溶液氧化 | B. | 能使溴水发生加成反应而褪色 | ||
| C. | 能发生水解反应 | D. | 易溶于水,也易溶于有机溶剂 |