题目内容
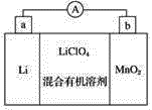
【题目】锂锰电池的体积小、性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质是LiClO4,溶于混合有机溶剂中,金属锂离子(Li+)通过电解质迁移入二氧化锰晶格中,生成LiMnO2。
回答下列问题:
(1)外电路的电流方向是由________极流向________极(填字母)。
(2)电池的正极反应式为___________。
(3)是否可用水代替电池中的混合有机溶剂________(填“是”或“否”),原因是_______。
【答案】b a MnO2+e-+Li+=LiMnO2 否 电极锂是活泼金属,能与水反应
【解析】
根据原电池原理及图示电池构造判断电池正负极,书写电极反应;根据电极的性质及电解质溶液的性质分析解答。
在锂锰电池中,金属锂为负极(a极),电极反应式为Li-e-![]() Li+;二氧化锰为正极(b极),电极反应式为MnO2+e-+Li+
Li+;二氧化锰为正极(b极),电极反应式为MnO2+e-+Li+![]() LiMnO2;在其外电路中,电子由负极(a极)流向正极(b极),而电流方向则由正极(b极)流向负极(a极);负极材料锂是活泼的金属,能与水发生反应,不能用水代替电池中的混合有机溶剂。故答案为:b ;a;MnO2+e-+Li+=LiMnO2;电极锂是活泼金属,能与水反应。
LiMnO2;在其外电路中,电子由负极(a极)流向正极(b极),而电流方向则由正极(b极)流向负极(a极);负极材料锂是活泼的金属,能与水发生反应,不能用水代替电池中的混合有机溶剂。故答案为:b ;a;MnO2+e-+Li+=LiMnO2;电极锂是活泼金属,能与水反应。

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目