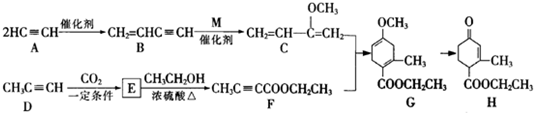
题目内容
17.如图为氢氧燃料电池原理示意图,下列叙述不正确的是( )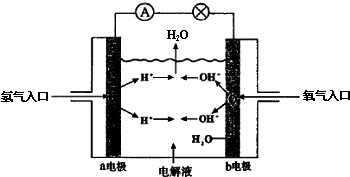
| A. | a电极是负极 | B. | b电极上发生氧化反应 | ||
| C. | 该电池工作时化学能转化为电能 | D. | 该电池的总反应为2H2+O2═2H2O |
分析 氢氧燃料电池中,氢气易失电子发生氧化反应,所以通入氢气的电极是负极,氧气易得电子发生还原反应,所以通入氧气的电极是正极,总反应为2H2+O2═2H2O,据此分析.
解答 解:A、氢气发生氧化反应,负极发生氧化反应,所以a电极是负极,故A正确;
B、b电极为正极,发生还原反应,故B错误;
C、原电池是把化学能转化为电能的装置,故C正确;
D、该电池的工作原理实质是氢气的燃烧反应,所以总反应为2H2+O2=2H2O,故D正确;
故选B.
点评 本题考查了原电池的工作原理、正负极的判断、发生的反应类型、能量的转化、电池反应方程式,题目难度不大.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
8.能用分液漏斗进行分离的一组物质是( )
| A. | 苯和硝基苯 | B. | 丙酸甲酯和水 | C. | 乙酸乙酯和乙酸 | D. | 溴苯和溴 |
5.下列化学用语表达正确的是( )
| A. | 一氯乙烷的结构式CH3Cl | B. | 丁烷的结构简式CH3(CH2)2CH3 | ||
| C. | 四氯化碳的电子式 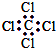 | D. | 苯的分子式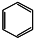 |
12.用下列实验装置进行的实验,能达到相应的实验目的是( )
| A. | 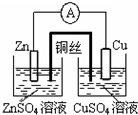 铜锌原电池 | B. | 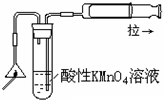 检验火柴头燃烧产生的SO2 | ||
| C. |  分液操作 | D. | 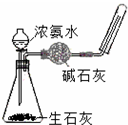 制取氨气 |
2.下列关于常见有机物的说法不正确的是 ( )
| A. | 食用植物油水解均可生成甘油 | |
| B. | 聚丙烯能使溴水褪色 | |
| C. | 苯和浓硝酸反应生成硝基苯,乙酸和乙醇反应生成乙酸乙酯,二者反应类型相同 | |
| D. | 向蔗糖水解后的溶液中加新制的Cu(OH)2悬浊液,加热到沸腾即可验证水解产物葡萄糖 |
9.下列有关氯气的叙述中,正确的是( )
| A. | 工业上常用MnO2和浓盐酸共热来制取氯气 | |
| B. | 新制氯水可使蓝色石蕊试纸先变红后褪色 | |
| C. | 在氧化还原反应中,Cl2只能作氧化剂 | |
| D. | 若提供含0.4 mol HCl的浓盐酸,MnO2过量,则可制得标准状况下氯气2.24 L |
6.分子式为C5H9O2Cl,属于卤代酯且能发生银镜反应的同分异构体共有( )
| A. | 10种 | B. | 11种 | C. | 12种 | D. | 13种 |
7.下列物质进行一氯取代反应,产物只有两种的是( )
| A. | (CH3)2CHCH2CH2CH3 | B. | (CH3CH2)2CHCH3 | C. | (CH3)2CHCH(CH3)2 | D. | (CH3)3CCH2CH3 |
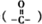 外,还含有的官能团名称是碳碳双键和酯基;
外,还含有的官能团名称是碳碳双键和酯基;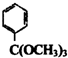 .
.