题目内容
13. 请认真观察如图,然后回答问题:
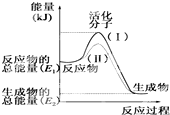
请认真观察如图,然后回答问题:(1)图中所示反应是放热(填“吸热”或“放热”)反应,该反应的△H=(E2-E1)KJ/mol(用含E1、E2的代数式表示).
(2)下列4个反应中,符合示意图描述的反应的是C.
a.盐酸与NaOH反应 b.Na与H2O反应生成H2
c.铝热反应 d.灼热的碳与CO2反应
(3)途径(Ⅱ)与途径(Ⅰ)相比改变的措施可能是加入催化剂.
分析 (1)依据图象分析反应物的能量大于生成物的能量,反应放热;在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才能发生化学反应,反应需要能量;反应的焓变=生成物的能量-反应物的能量;
(2)在上图所示的化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才能发生化学反应,反应需要能量,需要能量的放热反应;
(3)途径(Ⅱ)与途径(Ⅰ)相比改变活化能降低,改变的措施可能是加入催化剂.
解答 解:(1)依据图象分析反应物的能量大于生成物的能量,反应放热;反应的焓变=生成物的能量-反应物的能量,即△H=(E2-E1)kJ•mol-1,
故答案为:放热;(E2-E1)kJ•mol-1;
(2)在上图所示的化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才能发生化学反应,反应需要能量,需要能量的放热反应,只有C,铝热反应符合上图所示情况;
故答案为:C;
(3)途径(Ⅱ)与途径(Ⅰ)相比改变活化能降低,改变的措施可能是加入催化剂;
故答案为:加入催化剂.
点评 本题考查了化学反应的能量变化与反应的焓变关系的分析判断,反应活化能的判断计算,图象的综合应用,读懂图象,焓变和活化能计算方法的理解是解题的关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.利用铜萃取剂M,通过如下反应实现铜离子的富集:

(1)M与W(分子结构如图)相比,M的水溶性小,更利于Cu2+的萃取.M水溶性小的主要原因是M能形成分子内氢键,使溶解度减小.
(2)基态Cu2+的外围电子排布式为3d9,Cu2+等过渡元素水合离子是否有颜色与原子结构有关,且存在一定的规律.判断Sc3+、Zn2+的水合离子为无色的依据是3d轨道上没有未成对电子(3d轨道上电子为全空或全满).

(1)M与W(分子结构如图)相比,M的水溶性小,更利于Cu2+的萃取.M水溶性小的主要原因是M能形成分子内氢键,使溶解度减小.
(2)基态Cu2+的外围电子排布式为3d9,Cu2+等过渡元素水合离子是否有颜色与原子结构有关,且存在一定的规律.判断Sc3+、Zn2+的水合离子为无色的依据是3d轨道上没有未成对电子(3d轨道上电子为全空或全满).
| 离子 | Sc3+ | Ti3+ | Fe2+ | Cu2+ | Zn2+ |
| 颜色 | 无色 | 紫红色 | 浅绿色 | 蓝色 | 无色 |
18.甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H=+49.0kJ•mol-1
②CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)△H=-192.9kJ•mol-1
下列说法正确的是( )
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H=+49.0kJ•mol-1
②CH3OH(g)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)△H=-192.9kJ•mol-1
下列说法正确的是( )
| A. | CH3OH的燃烧热为192.9 kJ•mol-1 | |
| B. | 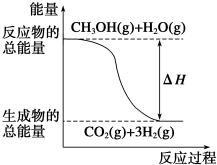 反应①中的能量变化如图所示 | |
| C. | CH3OH转变成H2的过程一定要吸收能量 | |
| D. | 根据②推知反应CH3OH(l)+$\frac{1}{2}$O2(g)═CO2(g)+2H2(g)的△H>-192.9 kJ•mol-1 |
5.在防止禽流感疫情时,防疫部门大量使用了含氯类消毒剂,其中氯胺是一种长效缓释的有机氯消毒剂,有强氧化性,其杀菌能力是一般含氯消毒剂的4-5倍,下列有关氯胺(NH2Cl)的说法中一定不正确的是( )
| A. | 氯胺水解产物最初为羟胺(NH2OH)和HCl | |
| B. | 氯胺在一定条件下可与乙烯加成得H2NCH2CH2Cl | |
| C. | 氯胺的消毒原理与漂白粉相似 | |
| D. | 氯胺的电子式为 |
2.某同学参阅了“84消毒液”说明中的配方,欲用NaClO固体配制480mL含NaClO 25%,密度为1.19g/cm3的消毒液.下列说法正确的是( )
| A. | 配制过程只需要三种仪器即可完成 | |
| B. | 容量瓶用蒸馏水洗净后必须烘干才能用于溶液的配制 | |
| C. | 所配得的NaClO消毒液在空气中光照,久置后溶液中NaClO的物质的量浓度减小 | |
| D. | 需要称量的NaClO固体的质量为140 g |
3.稀土元素是指元素周期表中原子序数为57到71的15种镧系元素,以及与镧系元素化学性质相似的钪(Sc)和钇(Y)共17 种元素.稀土有“工业维生素”的美称,如今已成为极其重要的战略资源.
几种稀土元素的电离能(单位:kJ•mol-1)
(1)离子化合物 Na3[Sc(OH)6]中,存在的作用力除离子键外还有共价键和配位键.
(2)Sm(钐)的单质与1,2-二碘乙烷可发生如下反应:Sm+ICH2CH2I→SmI2+CH2=CH2.
ICH2CH2I中碳原子杂化轨道类型为sp3,1mol CH2=CH2中含有的σ键数目为5NA.常温下1,2-二碘乙烷为液体而乙烷为气体,其主要原因是二碘乙烷的相对分子质量较大,分子间作用力较强,沸点相对较高.
(3)PrO2(二氧化镨)的晶体结构与CaF2相似,晶胞中Pr(镨)原子位于面心和顶点.则PrO2(二氧化镨)的晶胞中有8个氧原子.
(4)Ce(铈)单质为面心立方晶体,其胞参数为a=516pm.晶胞中Ce(铈)原子的配位数为12,列式表示Ce(铈)单质的密度:$\frac{4×140}{6.02×1{0}^{23}×({516×1{0}^{-10})}^{3}}$g•cm-3(不必计算出结果).
几种稀土元素的电离能(单位:kJ•mol-1)
| 元素 | I1 | I2 | I3 | I1+I2+I3 | I4 |
| Sc(钪) | 633 | 1235 | 2389 | 4257 | 7019 |
| Y(钇) | 616 | 1181 | 1980 | 3777 | 5963 |
| La(镧) | 538 | 1067 | 1850 | 3455 | 4819 |
| Ce(铈) | 527 | 1047 | 1949 | 3523 | 3547 |
(2)Sm(钐)的单质与1,2-二碘乙烷可发生如下反应:Sm+ICH2CH2I→SmI2+CH2=CH2.
ICH2CH2I中碳原子杂化轨道类型为sp3,1mol CH2=CH2中含有的σ键数目为5NA.常温下1,2-二碘乙烷为液体而乙烷为气体,其主要原因是二碘乙烷的相对分子质量较大,分子间作用力较强,沸点相对较高.
(3)PrO2(二氧化镨)的晶体结构与CaF2相似,晶胞中Pr(镨)原子位于面心和顶点.则PrO2(二氧化镨)的晶胞中有8个氧原子.
(4)Ce(铈)单质为面心立方晶体,其胞参数为a=516pm.晶胞中Ce(铈)原子的配位数为12,列式表示Ce(铈)单质的密度:$\frac{4×140}{6.02×1{0}^{23}×({516×1{0}^{-10})}^{3}}$g•cm-3(不必计算出结果).


 其反应类型是加聚反应
其反应类型是加聚反应