题目内容
5.下列各表中的数字代表的是原子序数,表中数字所表示的元素与它们在元素周期表中的位置相符的是( )| A. |
| B. |
| C. |
| D. |
|
分析 根据元素周期表的结构:相邻两个周期同主族元素的原子序数相差2、8、18、32,以此判断同族中位置关系.同周期元素根据原子序数判断位置关系,据此来分析.注意第三列镧系、锕系,长周期第ⅡA族、第ⅢA族之间有10个空列为7个副族和1个Ⅷ族.
解答 解:A、3号和6号元素之间相差很多个族,即12号的镁和6号的C在周期表中不相邻,故A错误;
B、5号和15号元素的原子不在同一主族,故B错误;
C、1号和11号中间还有3号元素,故C错误;
D、O、Cl、Ne、Kr的位置关系是正确的,故D正确;
故选D.
点评 本题考查元素周期表的结构及应用,为高频考点,把握元素的位置、原子序数等为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
4.下列物质中,既含有极性键又含有非极性键的离子化合物是( )
| A. | Na2S2O8 | B. | NH4HCO3 | C. | H2O2 | D. | NaOH |
16.为检验溶液中是否含有Cl-,某同学采用向溶液中先加HNO3,再加AgNO3,溶液的实验方案,若有白色沉淀生成,则证明有Cl-.对此结论,有人提出了质疑,设计了如下探究性实验.
实验一:向Na2SO4溶液中滴加AgNO3溶液
(1)实验一中产生沉淀的离子方程式为2Ag++SO42-═Ag2SO4↓.
(2)学生设计了如下表格,对实验一内容进行理论计算,请帮他完成表格.(表中不要留空格).
[25℃时Ksp(Ag2SO4)=1.2×10-5,Ksp(AgCl)=1.8×10-10]
若向l mL某溶液中加入3滴0.1mol/L AgNO3溶液,分析上面数据,判断下列说法正确的是AD (填字母序号).
A.混合液中c(SO42-)=0.1mol/L时不会产生Ag2SO4沉淀
B.混合液中c(SO42-)=1mol/L时不会产生Ag2SO4沉淀
c.无论SO42-浓度大小都会产生Ag2SO4沉淀
D.若使用0.01mol/L AgNO3溶液,可基本排除SO42-对Cl-检验构成的干扰
(3)将实验一中编号③中的理论计算结果与现象对照,发现理论上大部分Ag+应该形成沉淀,这与“有些许浑浊”的现象相矛盾.为探究真相,在实验一的基础上继续设计了以下实验.
实验二:
对于Ag2SO4溶于硝酸的原因提出了如下假设,请完成假设一.(已知:H2SO4=H++HSO4-、HSO4-=H++SO42-;假设二可能的原因是NO3-与Ag+形成配位化合物)
假设一:H+对Ag2SO4溶解起作用.
假设二:NO3-对Ag2SO4溶解起作用.
(4)从下列限选试剂中选择适当试剂并设计实验方案,分别验证假设一和假设二是否成立.请 写出实验步骤和结论.(限选试剂:Ag2SO4固体、浓HNO3、NaNO3饱和溶液、CaSO4固体)①取少量CaSO4固体于试管中,加入一定量浓HNO3,充分振荡.若沉淀溶解,说明假设一成立.
②取少量Ag2SO4固体于试管中,加入一定量NaNO3饱和溶液,充分振荡.若沉淀溶解,说明假设二成立
(5)通过(4)的实验,若证实假设一成立,请用平衡理论解释Ag2SO4溶解的原因Ag2SO4固体在水中存在平衡:Ag2SO4(s)?2Ag+(aq)+SO42-(aq),H+与SO42-结合生成HSO4-,SO42-浓度降低,平衡正向移动,Ag2SO4不断溶解.
实验一:向Na2SO4溶液中滴加AgNO3溶液
| 编号 | Na2S04溶液 | AgN03溶液 | 现象 | ||
| 体积/mL | 浓度/(mol•L-1) | 体积/滴 | 浓度/(mol•L-1) | ||
| ① | 1 | l | 3 | 2 | 出现大量白色沉淀 |
| ② | 1 | 1 | 3 | 0.5 | 出现少量白色沉淀 |
| ③ | 1 | 1 | 3 | 0.1 | 有些许浑浊 |
| ④ | 1 | 1 | 3 | 0.0l | 无明显变化 |
(2)学生设计了如下表格,对实验一内容进行理论计算,请帮他完成表格.(表中不要留空格).
[25℃时Ksp(Ag2SO4)=1.2×10-5,Ksp(AgCl)=1.8×10-10]
| 编号 | AgNO3浓度/(mol•L-1) | 稀释后Ag+浓度/(mol•L-1) | 混合液中SO42-的最小理论检出浓度/(mol•L-1) |
| ① | 2 | 0.2 | 0.0003 |
| ② | 0.5 | 0.0048 | |
| ③ | 0.1 | 0.0l | 0.12 |
| ④ | 0.001 |
A.混合液中c(SO42-)=0.1mol/L时不会产生Ag2SO4沉淀
B.混合液中c(SO42-)=1mol/L时不会产生Ag2SO4沉淀
c.无论SO42-浓度大小都会产生Ag2SO4沉淀
D.若使用0.01mol/L AgNO3溶液,可基本排除SO42-对Cl-检验构成的干扰
(3)将实验一中编号③中的理论计算结果与现象对照,发现理论上大部分Ag+应该形成沉淀,这与“有些许浑浊”的现象相矛盾.为探究真相,在实验一的基础上继续设计了以下实验.
实验二:
| 编号 | AgNO3溶液 浓度/(mol•L-1) | 现象 | 向沉淀中滴加硝酸后的现象 |
| ① | 2 | 出现大量白色沉淀 | 滴加稀硝酸,沉淀大量溶解;改加浓硝酸,沉淀较快消失 |
| ② | 0.5 | 出现少量白色沉淀 | 滴加稀硝酸,沉淀基本消失 |
假设一:H+对Ag2SO4溶解起作用.
假设二:NO3-对Ag2SO4溶解起作用.
(4)从下列限选试剂中选择适当试剂并设计实验方案,分别验证假设一和假设二是否成立.请 写出实验步骤和结论.(限选试剂:Ag2SO4固体、浓HNO3、NaNO3饱和溶液、CaSO4固体)①取少量CaSO4固体于试管中,加入一定量浓HNO3,充分振荡.若沉淀溶解,说明假设一成立.
②取少量Ag2SO4固体于试管中,加入一定量NaNO3饱和溶液,充分振荡.若沉淀溶解,说明假设二成立
(5)通过(4)的实验,若证实假设一成立,请用平衡理论解释Ag2SO4溶解的原因Ag2SO4固体在水中存在平衡:Ag2SO4(s)?2Ag+(aq)+SO42-(aq),H+与SO42-结合生成HSO4-,SO42-浓度降低,平衡正向移动,Ag2SO4不断溶解.
10.如图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为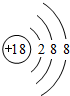 .
.
(2)地壳中含量最多的金属元素是Al;写出②与④按1:1形成的化合物的电子式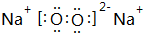 ,其中含有的化学键是离子键、共价键.
,其中含有的化学键是离子键、共价键.
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH.
(4)写出③、⑦、⑧对应的简单阴离子的还原性由强到弱的次序S2->Cl->F-
(5)④的最高价氧化物的水化物和⑤的最高价氧化物相互反应的离子方程式:Al2O3+2OH-=2AlO2-+H2O
(6)⑤和⑧组成的化合物中有共价键(化学键类型).
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 四 | ⑩ |
 .
.(2)地壳中含量最多的金属元素是Al;写出②与④按1:1形成的化合物的电子式
 ,其中含有的化学键是离子键、共价键.
,其中含有的化学键是离子键、共价键.(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH.
(4)写出③、⑦、⑧对应的简单阴离子的还原性由强到弱的次序S2->Cl->F-
(5)④的最高价氧化物的水化物和⑤的最高价氧化物相互反应的离子方程式:Al2O3+2OH-=2AlO2-+H2O
(6)⑤和⑧组成的化合物中有共价键(化学键类型).
17.运用元素周期律分析下面推断,其中错误的是( )
| A. | 铍(Be)的氧化物的水化物可能具有两性 | |
| B. | 砹(At)为有色固体,HAt不稳定,AgAt感光性很强,但不溶于水也不溶于酸 | |
| C. | 硫酸锶(SrSO4)是难溶于水的白色固体 | |
| D. | 硒化氢(H2Se)是有色、有毒的气体,比H2S稳定 |
14.下列各个装置中能组成原电池的是( )
| A. | 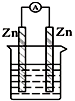 稀硫酸 | B. | 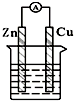 CuSO4溶液 | ||
| C. | 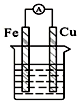 酒精溶液 | D. | 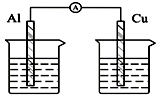 稀硫酸 稀硫酸 |
15.下列物质中,既含有离子键,又含有共价键的是( )
| A. | Na2O | B. | MgCl2 | C. | NaCl | D. | NaOH |