题目内容
4.下列物质中,既含有极性键又含有非极性键的离子化合物是( )| A. | Na2S2O8 | B. | NH4HCO3 | C. | H2O2 | D. | NaOH |
分析 由不同非金属原子之间形成的为极性共价键,由相同非金属原子形成的共价键为非极性共价键,阴、阳离子之间的静电作用叫离子键,以此解答.
解答 解:A、过氧硫酸钠(Na2S2O8)是S-O-O-S,含有过氧非极性键,钠与过氧硫酸离子之间的离子键,所以符合条件,故A正确;
B、碳酸氢铵中存在离子键和极性共价键,不符合条件,故B错误;
C、过氧化氢中只存在非极性和极性共价键,不符合条件,故C错误;
D、氢氧化钠中存在离子键和极性共价键,不符合条件,故D错误;
故选A.
点评 本题考查共价键知识,注意极性共价键、非极性共价键的区别以及判断方法,注意相关基础知识的积累,如果不知过氧硫酸钠中存在非极性共价键可以用排除法解决,难度不大.

练习册系列答案
相关题目
14.下列有关实验的说法正确的是( )
| A. | 用湿润的pH试纸测溶液的pH | |
| B. | 实验室制备干燥纯净的氯气时,气体先通过饱和食盐水再通过浓硫酸 | |
| C. | 用玻璃棒在过滤器上搅拌以加速AgCl沉淀的洗涤 | |
| D. | 中和滴定实验中,锥形瓶用蒸馏水洗净后未干燥,测定结果偏低 |
19.下列实验不能达到目的是( )
| A. | 用KSCN溶液检验Fe2+ | B. | 用湿润的红色石蕊试纸检验氨气 | ||
| C. | 用湿润的淀粉碘化钾试纸检验氯气 | D. | 用硝酸酸化的AgNO3溶液检验Cl- |
9.实验室用浓盐酸与浓硫酸混合快速制取HCl.下列解释正确的是( )
| A. | 浓硫酸是高沸点的酸,通过它与浓盐酸反应制取低沸点的酸 | |
| B. | 通过改变温度和浓度等条件,利用平衡移动原理制取HCl | |
| C. | 两种强酸混合,溶解度会相互影响,低溶解度的物质析出 | |
| D. | 浓硫酸的浓度(98%)远大于浓盐酸的浓度(37%),高浓度的酸制取低浓度的酸 |
16.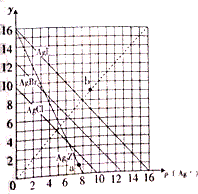 卤化银AgX及Ag2Z的沉淀溶解平衡曲线如图所示,已知横坐标p(Ag+)=-lgc(Ag+),纵坐标y=-lgc(X-)或-lgc(Z2-).下列说法正确的是( )
卤化银AgX及Ag2Z的沉淀溶解平衡曲线如图所示,已知横坐标p(Ag+)=-lgc(Ag+),纵坐标y=-lgc(X-)或-lgc(Z2-).下列说法正确的是( )
 卤化银AgX及Ag2Z的沉淀溶解平衡曲线如图所示,已知横坐标p(Ag+)=-lgc(Ag+),纵坐标y=-lgc(X-)或-lgc(Z2-).下列说法正确的是( )
卤化银AgX及Ag2Z的沉淀溶解平衡曲线如图所示,已知横坐标p(Ag+)=-lgc(Ag+),纵坐标y=-lgc(X-)或-lgc(Z2-).下列说法正确的是( )| A. | 该温度下Ag2Z的Ksp约为1×10-8 | |
| B. | a点可表示AgCl的过饱和溶液 | |
| C. | b点可表示AgI的过饱和溶液,且c(Ag+)=c(I-) | |
| D. | 该温度下AgCl、AgBr形成的混合溶液的饱和溶液中:c(Cl-)<c(Br-) |
4.${\;}_{27}^{60}$Co是γ放射源,${\;}_{27}^{60}$Co可用于农作物的诱变育种,我国用该方法培育出了许多农作物新品种.对原子的叙述不正确的是( )
| A. | 质量数是60 | B. | 质子数是 27 | C. | 中子数是33 | D. | 电子数是33 |
5.下列各表中的数字代表的是原子序数,表中数字所表示的元素与它们在元素周期表中的位置相符的是( )
| A. |
| B. |
| C. |
| D. |
|