题目内容
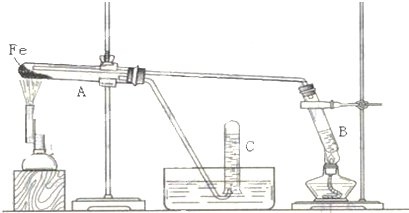
6. 请你利用所学反应原理知识解决下列问题:
请你利用所学反应原理知识解决下列问题:(1)若已知两个反应:
①C(s)+2H2(g)═CH4(g)△H1=a kJ•mol-1;
②C(s)+$\frac{1}{2}$O2(g)═CO(g)△H2=b kJ•mol-1;
则2CH4(g)+O2(g)═2CO(g)+4H2(g)△H=2(b-a)kJ•mol-1(用含a、b的式子表示)
(2)碱性镁锰干电池是新开发的一种干电池,比普通锌锰干电池具有更加优越的性能,具有较大应用前景,其工作时总反应为:Mg+2MnO2+H2O═Mg(OH)2+Mn2O3;则工作时,正极发生还原反应(填反应类型),写出负极的电极反应式:Mg+2OH--2e-=Mg(OH)2;
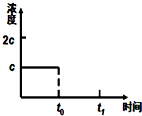
(3)在一定温度下1L的密闭容器放入足量草酸钙(固体所占体积忽略不计)发生反应:CaC2O4(s)═CaO(s)+CO(g)+CO2(g),若前5min 内生成CaO的质量为11.2g,则该段时间内v(CO)=0.04mol•L-1•min-1;若某时刻达到平衡时c(CO2)=c;t0时刻,将容器体积缩小为原来的一半并固定不变,在t1时刻再次达到平衡,请在如图中画出t0以后此体系中CO2的浓度随时间变化的图象;
(4)某温度下数据:草酸(H2C2O4)的K1=5.4×10-2,K2=5.4×10-5;醋酸的K=1.75×10-5;碳酸的 K1=4.2×10-7,K2=4.5×10-11;Ksp(CaC2O4)=5.0×10-9;Ksp(CaCO3)=2.5×10-9
①用醋酸溶液鉴别CaC2O4和CaCO3两种白色固体的实验现象是一种固体溶解同时产生气泡逸出,另一种固体无现象;
②向0.6mol/L的Na2CO3溶液中加入足量 CaC2O4粉末后(忽略溶液体积变化),充分搅拌,发生反应:CO${\;}_{3}^{2-}$(aq)+CaC2O4(s)$\sqrt{2}{E_m}_{\;}$CaCO3(s)+C2O${\;}_{4}^{2-}$(aq),静置后沉淀转化达到平衡,求此时溶液中的c(C2O${\;}_{4}^{2-}$)=0.4 mol•L?1(不考虑其他诸如水解之类副反应,写出计算过程).
分析 (1)由盖斯定律可知,②×2-①×2得2CH4(g)+O2(g)═2CO(g)+4H2(g)以此计算△H;
(2)正极是MnO2得到电子发生还原反应生成Mn2O3,负极镁失电子生成的镁离子和氢氧根结合生成氢氧化镁沉淀;
(3)前5min 内生成CaO的质量为11.2g,n(CO)=n(CaO)=$\frac{11.2g}{56g/mol}$=0.2mol,则v(CO)=$\frac{0.2mol}{1L•5min}$=0.04mol•L-1•min-1;温度不变,平衡常数不变,t0时刻,将容器体积缩小为原来的一半并固定不变,c(CO2)=2c,在t1时刻再次达到平衡时,c(CO2)=c,作图即可;
(4)①醋酸的酸性大于碳酸的酸性,小于草酸的酸性,故醋酸与CaC2O4不反应,与CaCO3反应有气泡逸出;
②该反应的K=$\frac{{c({C_2}O_4^{2-})}}{{c(CO_3^{2-})}}$=$\frac{{c({C_2}O_4^{2-})•c(C{a^{2+}})}}{{c(CO_3^{2-})•c(C{a^{2+}})}}$=$\frac{{Ksp(Ca{C_2}{O_4})}}{{Ksp(CaC{O_3})}}$=$\frac{{5.0×{{10}^{-9}}}}{{2.5×{{10}^{-9}}}}$=2.0,设c(CO32-)转化了x,则生成c(C2O42-)=x,剩余c(CO32-)=(0.6-x),
结合K的表达式计算.
解答 解:(1)①C(s)+2H2(g)═CH4(g)△H1=a kJ•mol-1;
②C(s)+$\frac{1}{2}$O2(g)═CO(g)△H2=b kJ•mol-1;
依据盖斯定律:②×2-①×2得2CH4(g)+O2(g)═2CO(g)+4H2(g)△H=2(b-a)kJ•mmol-1;
故答案为:2(b-a)kJ•mmol-1;
(2)正极是MnO2得到电子发生还原反应生成Mn2O3,负极镁失电子生成的镁离子和氢氧根结合生成氢氧化镁沉淀,Mg-2e-+2OH-=Mg(OH)2,
故答案为:还原;Mg+2OH--2e-=Mg(OH)2;
(3)前5min 内生成CaO的质量为11.2g,n(CO)=n(CaO)=$\frac{11.2g}{56g/mol}$=0.2mol,则v(CO)=$\frac{0.2mol}{1L•5min}$=0.04mol•L-1•min-1;温度不变,平衡常数不变,t0时刻,将容器体积缩小为原来的一半并固定不变,c(CO2)=2c,在t1时刻再次达到平衡时,c(CO2)=c,作图如下: ,
,
故答案为:0.04mol•L-1•min-1; ;
;
(4)①醋酸的酸性大于碳酸的酸性,小于草酸的酸性,故醋酸与CaC2O4不反应,与CaCO3反应有气泡逸出;
故答案为:一种固体溶解同时产生气泡逸出,另一种固体无现象;
②该反应的K=$\frac{{c({C_2}O_4^{2-})}}{{c(CO_3^{2-})}}$=$\frac{{c({C_2}O_4^{2-})•c(C{a^{2+}})}}{{c(CO_3^{2-})•c(C{a^{2+}})}}$=$\frac{{Ksp(Ca{C_2}{O_4})}}{{Ksp(CaC{O_3})}}$=$\frac{{5.0×{{10}^{-9}}}}{{2.5×{{10}^{-9}}}}$=2.0,
设c(CO32-)转化了x,则生成c(C2O42-)=x,剩余c(CO32-)=(0.6-x),
可得方程:$\frac{x}{(0.6-x)}$=2.0,解得x=0.4 mol•L?1;
故答案为:0.4 mol•L?1.
点评 本题考查盖斯定律、原电池原理的应用、弱酸的性质等知识,综合性较强,难度中等.

 春雨教育同步作文系列答案
春雨教育同步作文系列答案| A. | 中性溶液中:Fe3+、K+、Cl-、SO42- | |
| B. | 在澄清透明溶液中:NH4+、Cu2+、Cl-、SO42- | |
| C. | 酸性溶液中:Na+、K+、ClO-、NO3- | |
| D. | 0.1 mol•L-1 KMnO4溶液:Na+、K+、Cl-、SO32- |
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | … | 23 | 24 |
| C2H6 | C2H6O | C2H4O2 | C3H8 | C3H8O | C3H6O2 | C4H10 | … | M | N |
| A. | M为C9H20O | B. | N为C9H18O2 | ||
| C. | M、N均可发生加成反应 | D. | M、N均可能发生取代反应 |
| A. | 将pH=4的CH3COOH溶液加水稀释10倍,溶液中各离子浓度均减小 | |
| B. | 用CH3COOH溶液滴定等物质的量浓度NaOH溶液至pH=7,V(CH3COOH)<V(NaOH)溶液 | |
| C. | 向0.2mol/L的盐酸溶液中加入等体积0.1mol•L-1的NH3•H2O溶液:c(Cl-)+c(OH-)=c(H+)+c(NH3•H2O) | |
| D. | 在含0.1mol NaHSO4溶液中:c(H+)=c(SO42-)+c(OH-) |
 氨气是一种重要的化工原料,在工农业中都有广泛的应用.
氨气是一种重要的化工原料,在工农业中都有广泛的应用.(1)NH3和CO2在120℃和催化剂的作用下可以合成尿素,反应方程式如下:2NH3(g)+CO2(g)?CO(NH2)2(s)+H2O(g).某实验小组向一个容积不变的真空密闭容器中充入CO2与NH3合成尿素.在恒定温度下,混合气体中NH3的含量随时间的变化关系如图所示(该条件下尿素为固体).A点的正反应速率v正(CO2)大于B点的逆反应速率v逆(CO2)(填“大于”、“小于”或“等于”),NH3的平衡转化率为75%.
(2)氨基甲酸铵(NH2COONH4)是合成尿素过程中的中间产物.现将体积比为2:1的NH3和CO2混合气体充入一个容积不变的真空密闭容器中,在恒定温度下使其发生反应并达到平衡:2NH3(g)+CO2(g)?NH2COONH4(s).实验测得在不同温度下的平衡数据如下表:
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡气体总浓度 (10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
②若从已达平衡状态的上述容器中分离出少量的氨基甲酸铵晶体,反应物的转化率将不变(填“增大”、“减小”或“不变”).
(3)向含a mol NH4NO3的溶液中滴加b L氨水后溶液恰好呈中性,则滴加氨水的过程中水的电离平衡将
逆向(填“正向”、“不”或“逆向”)移动,所滴加氨水的浓度为$\frac{a}{200b}$mol•L-1(25℃时,NH3•H2O的电离平衡常数Kb=2×10-5)
| A. |  表示稀释冰醋酸过程中溶液导电性的变化曲线 | |
| B. |  曲线表示反应2SO2(g)+O2(g)═2SO3(g);△H<0 正、逆反应的平衡常数K随温度的变化 | |
| C. | 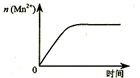 表示10 mL 0.01 mol•L-1 KMnO4 酸性溶液与过量的0.1 mol•L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化 | |
| D. |  a、b曲线分别表示反应CH2=CH2 (g)+H2(g)→CH3CH3(g);△H<0使用和未使用催化剂时,反应过程中的能量变化 |
| A. | MnO4-、Fe2+、K+、Cl- | B. | Ca2+、Na+、Cl-、SO42- | ||
| C. | Ca2+、Cl-、NO3-、K+ | D. | Ca2+、H+、OH-、CO32- |
| A. | CH3CH2OH→CH2=CH2↑+H2O | |
| B. | CH3CHBrCH3+NaOH→CH3CH=CH2↑+NaBr+H2O | |
| C. | 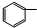 CHClCH2Cl+2NaOH→ CHClCH2Cl+2NaOH→ C≡CH+2NaCl+2H2O C≡CH+2NaCl+2H2O | |
| D. | 2CH3OH→CH3-O-CH3+H2O |