题目内容
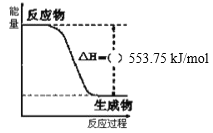
【题目】工业上在恒容密闭容器中用下列反应合成甲醇:CO(g)+2H2(g)![]() CH3OH(g)△H
CH3OH(g)△H
(1)该反应的平衡常数表达式为_______;
(2)如表所列数据是反应在不同温度下的化学平衡常数(K)
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
①由表中数据判断该反应的△H______0(填“>”、“=”或“<”);
②某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应10s后达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为____,用H2表示反应速率为_____,此时的温度为______;
(3)要提高CO的转化率,可以采取的措施是______;
a.升温 b.加入催化剂 c.增加CO的浓度
d.恒容充入H2 e.恒压充入惰性气体 f.分离出甲醇
【答案】K=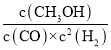 < 80% 0.16molL-1s-1 250℃ DEF
< 80% 0.16molL-1s-1 250℃ DEF
【解析】
(1)已知反应CO(g)+2H2(g)![]() CH3OH(g),该反应的平衡常数表达式K=
CH3OH(g),该反应的平衡常数表达式K=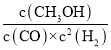 ;
;
(2)①温度升高,K减小,说明升高温度平衡向逆反应方向移动,则正反应为放热反应,即△H<0;
②达到平衡时测得c(CO)=0.2mol/L,则转化的CO的物质的量为2.0mol-0.2mol/L×2L=1.6mol,所以CO的转化率为![]() ×100%=80%,则:
×100%=80%,则:
CO(g)+2H2(g)![]() CH3OH(g)
CH3OH(g)
起始: 1mol/L 3mol/L 0
转化: 0.8mol/L 1.6mol/L 0.8mol/L
平衡: 0.2mol/L 1.4mol/L 0.8mol/L
所以:用H2表示反应速率为![]() =0.16molL-1s-1;
=0.16molL-1s-1;
K=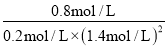 =2.041(mol/L)-2,温度应为250℃;
=2.041(mol/L)-2,温度应为250℃;
(3)A.升温,平衡向逆反应方向移动,CO的转化率的减小,故A错误;
B.加入催化剂,平衡不移动,转化率不变,故B错误;
C.增加CO的浓度,CO的转化率的减小,故C错误;
D.恒容充入H2,平衡向正反应方向移动,CO转化率增大,故D正确;
E.恒压充入惰性气体,分压减小,平衡向正反应方向移动,CO转化率增大,故E正确;
F.分离出甲醇,平衡向正反应方向移动,转化率增大,故F正确;
故答案为DEF。

【题目】某化学兴趣小组同学在查阅资料的基础上对乙醛与新制氢氧化铜的反应进行了探究。
(1)乙醛与新制氢氧化铜反应的化学方程式为________。
(查阅资料)i.乙醛在碱性条件下可发生缩合等反应生成有色物质;ii.溶液的酸碱性可能会影响物质的氧化性、还原性。
(初步探究)
序号 | 实验操作 | 实验现象 |
I | 向试管中加入4 mL 10 % NaOH溶液,滴入0.5 mL 水,加入0.5 mL 40 %乙醛溶液,振荡;在酒精灯上加热至沸腾后保持沸腾 | 无色溶液逐渐变黄,并变浑浊;加热后得黄色浊液,之后无明显变化 |
II | 向试管中加入4 mL 10 % NaOH溶液,滴入0.5 mL 2 %CuSO4溶液,振荡;加入0.5 mL 40 %乙醛溶液,振荡;在酒精灯上加热至沸腾后保持沸腾 | 蓝色浊液依次呈绿色、黄色、橙色,最终生成红色固体;之后无明显变化 |
III | 向试管中加入4 mL水,滴入0.5 mL 2 %CuSO4溶液,振荡;加入0.5 mL 40 %乙醛溶液,振荡;在酒精灯上加热至沸腾后保持沸腾 | 蓝色溶液无明显变化 |
(2)实验I的目的是________。
(3)甲同学为了检验实验II中红色固体的成分进行了如下实验:取少量红色固体于试管中,加入适量稀HNO3,振荡,观察到红色固体完全溶解,得蓝色溶液。甲同学认为,该实验现象说明实验II中反应生成了Cu。乙同学认为甲的观点不正确,理由是_____。
(深入探究)乙同学对比实验II和实验III,对实验II能够发生反应的原因提出了猜想:乙醛的还原性随着溶液碱性的增强而增强,并利用实验IV进行验证。
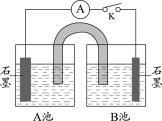
实验装置 | 序号 | A池试剂 | B池试剂 | 实验现象 |
| IV-1 | 0.2% CuSO4溶液 | Na2SO4溶液和40%乙醛溶液按体积比9:1混合 | 指针不偏转,A、B池中均无明显变化 |
IV-2 | 0.2% CuSO4溶液 |
(4)实验IV-1中,Na2SO4溶液的作用是________。
(5)实验IV-2中,B池中的试剂是________。
(6)根据实验现象,乙同学认为其猜想成立。乙同学观察到的实验现象是________。
(7)综合上述实验,小组同学经过深入讨论,认为除了乙同学的猜想外,与实验III相比,实验II能够发生反应的原因还可能有________和________。
【题目】(I)某烃A的相对分子质量为84。回答下列问题:
(1)物质的量相同,下列物质充分燃烧与A消耗氧气的量不相等的是(填序号)_____。
A.C7H12O2 B.C6H14 C.C6H14O D.C7H14O3
(2)若烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种。则A的结构简式为______________。
(3)若核磁共振氢谱显示链烃A有三组不同的峰,峰面积比为3:2:1,则A的名称为____。
(4)若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为_____________.
(II)有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的A为无色黏稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
实验步骤 | 实验结论 |
(1)称取A4.5g,升温使其汽化,测其密度是相同条件下H2的45倍。 | A的相对分子质量为:_____。 |
(2)将此4.5gA在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重2.7g和6.6g | A的分子式为:________。 |
(3)另取A4.5g,跟足量的NaHCO3粉末反应,生成1.12LCO2(标准状况),若与足量金属钠反应则生成1.12LH2(标准状况) | 写出A中含有的官能团____________、________。 |
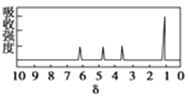
(4)A的核磁共振氢谱如下图: | 综上所述,A的结构简式为________ |