��Ŀ����
����Ŀ��(1) д����ԭ�ӵĵ����Ų�ʽ_____________��
(2) ��ͪ(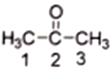 )������2��̼ԭ�ӵ��ӻ���ʽΪ__________����CS2��Ϊ�ȵ��������������__________(дһ��)��
)������2��̼ԭ�ӵ��ӻ���ʽΪ__________����CS2��Ϊ�ȵ��������������__________(дһ��)��
(3)��0.1mol[Cr(H2O)Cl]Cl2��H2O��ˮ��Һ��������������Һ��Ӧ����_______molAgCl������H2O���ӵļ��DZ�H2S���ӵļ��Ǵ�ԭ����_______ ��
(4) ��ͭ�����γɵ�һ�ֻ�����ľ����ṹ��ͼ��ʾ(�ڵ����ͭԭ��)��

���þ���Ļ�ѧʽΪ_______��
���������ڵ�4���ڵ���������γɵ����幹����_______��
�۾�������һ����ԭ�Ӿ����������ԭ����_______����
����֪�þ�����ܶ�Ϊ��g.cm-3�������ӵ�������ֵΪNA����þ�����ͭԭ�Ӻ���ԭ��֮�����̾���Ϊ_______pm(�г�����ʽ����)��
���𰸡� 1s22s22p63s23p63d84s2 ��[Ar]3d84s2 sp2�ӻ� SCN������OCN����CNO����N3-�ȣ� 0.2 ����ԭ�Ӱ뾶����С���縺�Ա������ˮ�����гɼ����ӶԸ���������ԭ�ӣ���ų����ô��Ǵ� CuCl ���������� 12 ![]() ��
��![]() ��1010
��1010
����������1������28��Ԫ�أ���ԭ�Ӻ�����28�����ӣ�����ԭ�Ӻ�������Ų����ɿɵ���ԭ�ӵĵ����Ų�ʽΪ��1s22s22p63s23p63d84s2 ��[Ar]3d84s2��
��2����ͪ(CH3COCH3)�ʻ��е�̼ԭ���γ���3���������¶Ե��ӣ�����Ϊsp2�ӻ���SCN-��OCN-��CNO-��N3-����CS2ԭ�Ӹ�����ͬ���۵�������ͬ����Ϊ�ȵ�������
��3��[Cr(H2O)Cl]Cl2��H2O�й�����3�������ӣ�����1������������ԭ�ӣ���2�������ӿ���Ag+��ϳ�AgCl���������Ժ�0.1mol[Cr(H2O)Cl]Cl2��H2O��ˮ��Һ��������������Һ��Ӧ����0.2molAgCl������H2O������H2S�������е�O��Sԭ�Ӷ���ȡ��sp3�ӻ�������2���µ��Ӷԣ�������ԭ�Ӱ뾶�����С���縺�Ա����ˮ�����гɼ����ӶԸ���������ԭ�ӣ���ų����ô��Ǵ���
��4���ٸþ���Ϊ��������������ԭ��ռ![]() ������ԭ��ռ
������ԭ��ռ![]() ���ڲ�ԭ��Ϊ�����������У����Ըþ����У�Clԭ�ӵ���ĿΪ��8��
���ڲ�ԭ��Ϊ�����������У����Ըþ����У�Clԭ�ӵ���ĿΪ��8��![]() +6��
+6��![]() =4��Cuԭ�ӵ���ĿΪ4����þ���Ļ�ѧʽΪCuCl�����ɾ����ṹ���Կ������þ�������ʯ�������ƣ����Խ������ڵ��ĸ��ڵ�����ӣ��������һ�����������������Ծ�������Clԭ��Ϊ�о�������8���������ø�Clԭ�ӣ�ÿ��Clԭ��������ĵ�Clԭ�Ӿ��������ÿ������Clԭ��Ϊ�����������ã�����ÿ����ԭ����Χ��֮�����������ԭ�Ӹ���Ϊ��3��8��
=4��Cuԭ�ӵ���ĿΪ4����þ���Ļ�ѧʽΪCuCl�����ɾ����ṹ���Կ������þ�������ʯ�������ƣ����Խ������ڵ��ĸ��ڵ�����ӣ��������һ�����������������Ծ�������Clԭ��Ϊ�о�������8���������ø�Clԭ�ӣ�ÿ��Clԭ��������ĵ�Clԭ�Ӿ��������ÿ������Clԭ��Ϊ�����������ã�����ÿ����ԭ����Χ��֮�����������ԭ�Ӹ���Ϊ��3��8��![]() =12�����辧���߳�Ϊacm����һ�����������Ϊa3cm3��һ�������к���4��Cuԭ�Ӻ�4��Clԭ�ӣ���1������������Ϊm=
=12�����辧���߳�Ϊacm����һ�����������Ϊa3cm3��һ�������к���4��Cuԭ�Ӻ�4��Clԭ�ӣ���1������������Ϊm=![]() g=
g=![]() g����Ϊ�ܶ�Ϊ��g.cm-3�����Ծ����ı߳�a=
g����Ϊ�ܶ�Ϊ��g.cm-3�����Ծ����ı߳�a=![]() cm��CuCl�ľ�������ʯ�������ƣ����Ըþ�����ͭԭ�Ӻ���ԭ��֮�����̾���Ϊ
cm��CuCl�ľ�������ʯ�������ƣ����Ըþ�����ͭԭ�Ӻ���ԭ��֮�����̾���Ϊ![]() ��
��![]() cm=
cm=![]() ��
��![]() ��101pm��
��101pm��

����Ŀ����ţ�̺ͽ�֭��ϣ���ţ�����̱��Ϊһ�ָ��й㶫��ɫ����Ʒ������ײ�̡�Ϊ������ţ�����������������ijͬѧ�ڲ�ͬ�¶ȵĵ���ţ���л���һЩ���ʽ�֭���۲�����15min�������Ƿ�����̣�������±�����ش��������⣺
�¶ȣ����� | 20 | 40 | 60 | 80 | 100 |
��� | 15min����δ�����̼��� | 14min����ȫ���� | 1min����ȫ���� | 1min����ȫ���� | 15min����δ�����̼��� |
��ע��������еĽ�֭�ظ�����ʵ�飬ţ�����κ��¶��¾��������̣�
��1��ʵ��֤�����ʽ�֭�к���һ��ø����������__��
��2��20����100��ʱ��15min����δ�����̼���˵��ø�Ļ��Խϵͣ���ԭ��ֱ���__��__��
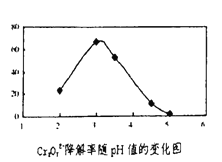
��3����60��ʱţ�����н�֭��û�н�֭������¶��������̣�����Ӧ���е�tʱ�������м��˽�֭����ͼ��ͼ������ȷ��ʾ�ӽ�֭��ţ��������ʱ��仯���Ƶ�������__��

��4��Ϊ���ʵ���ȷ�ȣ�ʵ��������ͬ�¶ȵĵ���ţ���л���һЩ���ʽ�֭��������Ӧע�����__��
��5����ͬѧ˵����ʵ�鲻�ܵó���֭ʹţ�����̵������¶ȣ���������������__��