题目内容
【题目】(1)一定条件下,平衡常数如下:
2NO2![]() N2O4 K1 NO2
N2O4 K1 NO2![]() 1/2N2O4K2 N2O4
1/2N2O4K2 N2O4![]() 2NO2 K3
2NO2 K3
推导K1与K2,K1与K3的关系分别为:______________。
(2)衡量催化剂的性能指标有:活性、选择性、稳定性、价格等。对于给定条件下反应物之间能够同时发生多个反应的情况,理想的催化剂可以大幅度提高目标产物在最终产物中的____(填“产率”、“比率”、转化率),催化剂的这种特性,称作它的________性。
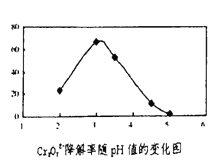
(3)溶液的pH对Cr2O72-降解率的影响如下图所示。
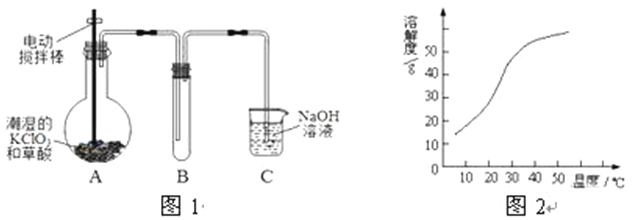
已知:Cu2O![]() Cu+CuSO4;
Cu+CuSO4;
酸性越大,Cr2O72-被还原率越大。
①由上右图可知,pH分别为2、3、4 时,Cr2O72-的降解率最好的是______,其原因是______。
②按右图加入10滴浓硫酸,溶液由橙黄色变为橙色,请结合化学用语用平衡移动原理解释其原因_____。
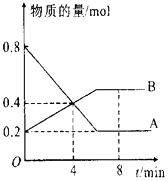
(4)一定条件下焦炭可以还原NO2,反应为:2NO2(g)+2C(s) ![]() N2(g)+2CO2(g)。在恒温的密闭容器下,6molNO2和足量C 发生该反应,测得平衡时NO2的物质的量与平衡总压的关系如图所示:
N2(g)+2CO2(g)。在恒温的密闭容器下,6molNO2和足量C 发生该反应,测得平衡时NO2的物质的量与平衡总压的关系如图所示:
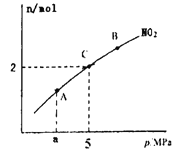
则C点NO2的转化率和C点时该反应的压强平衡常数Kp=(K,是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)分别为______、_______。
(5)已知由CO生成CO2的化学方程式为CO+O2![]() CO2+O。其正反应速率为v正=K正c(CO)·c(O2),逆反应速率为v逆=K逆c(CO2)·c(O),K正、K逆为速率常数。在2500K下,K正=1.21×105 L·s-1·mol-1,K逆=3.02×105L·s-1·mol-1。则该温度下上述反应的平衡常数K值为_______(保留小数点后一位小数)。
CO2+O。其正反应速率为v正=K正c(CO)·c(O2),逆反应速率为v逆=K逆c(CO2)·c(O),K正、K逆为速率常数。在2500K下,K正=1.21×105 L·s-1·mol-1,K逆=3.02×105L·s-1·mol-1。则该温度下上述反应的平衡常数K值为_______(保留小数点后一位小数)。
(6)利用水煤气合成二甲醚的三步反应如下:
①2H2(g) + CO(g) ![]() CH3OH(g); ΔH1
CH3OH(g); ΔH1
②CH3OH(g) ![]() CH2OCH3(g) + H2O(g); ΔH2
CH2OCH3(g) + H2O(g); ΔH2
③CO(g) + H2O(g) ![]() CO2(g) + H2(g); ΔH3
CO2(g) + H2(g); ΔH3
总反应: 3H2(g)+3CO(g) ![]() CH2OCH3(g)+CO2(g)的ΔH=_______。
CH2OCH3(g)+CO2(g)的ΔH=_______。
【答案】 K1=K22:K1=1/K3 比率 选择性 3 pH<2.5时Cu2O会歧化(转化)为Cu和Cu2+,所以不选pH=2;酸性越大,Cr2O72-被还原率越大,pH=3酸性强于pH=4的溶液,所以选择pH=3 溶液中存在 ,加入硫酸,c(H+)增大,平衡向逆反应方向移动c(Cr2O72-)增大 66.7% 5Mpa 0.4 【答题空10】2ΔH1+ΔH2+ΔH3
,加入硫酸,c(H+)增大,平衡向逆反应方向移动c(Cr2O72-)增大 66.7% 5Mpa 0.4 【答题空10】2ΔH1+ΔH2+ΔH3
【解析】(1)一定条件下,平衡常数如下:2NO2![]() N2O4 K1 NO2
N2O4 K1 NO2![]() 1/2N2O4K2 N2O4
1/2N2O4K2 N2O4![]() 2NO2 K3,K1=c(N2O4 )/c2(NO2)=[c0.5(N2O4 )/c(NO2)]2=K22;K1=c(N2O4 )/c2(NO2)=[c2(NO2)/c(N2O4 )]-1=1/K3,故K1与K2,K1与K3的关系分别为: K1=K22:K1=1/K3 ;
2NO2 K3,K1=c(N2O4 )/c2(NO2)=[c0.5(N2O4 )/c(NO2)]2=K22;K1=c(N2O4 )/c2(NO2)=[c2(NO2)/c(N2O4 )]-1=1/K3,故K1与K2,K1与K3的关系分别为: K1=K22:K1=1/K3 ;
(2)衡量催化剂的性能指标有:活性、选择性、稳定性、价格等。对于给定条件下反应物之间能够同时发生多个反应的情况,理想的催化剂可以大幅度提高目标产物在最终产物中的比率(填“产率”、“比率”、转化率),催化剂的这种特性,称作它的选择性。
(3)①由图可知,pH分别为2、3、4 时,Cr2O72-的降解率最好的是3,其原因是由图可知:pH<2.5时Cu2O会歧化(转化)为Cu 和Cu2+,故答案为:pH=3;pH<2.5时Cu2O会歧化(转化)为Cu 和Cu2+,所以不选pH=2;酸性越大,Cr2O72-被还原率越大,pH=3酸性强于pH=4的溶液,所以选择pH=3。
②按右图加入10滴浓硫酸,溶液由橙黄色变为橙色,请结合化学用语用平衡移动原理解释其原因溶液中存在Cr2O72-+H2O![]() 2CrO42-+2H+,加入硫酸,c(H+)增大,平衡向逆反应方向移动c(Cr2O72-)增大。
2CrO42-+2H+,加入硫酸,c(H+)增大,平衡向逆反应方向移动c(Cr2O72-)增大。
(4)6mol NO2和足量C发生该反应,设反应二氧化氮x,列三段式:
2NO2(g)+2C(s)![]() N2(g)+2CO2(g)
N2(g)+2CO2(g)
n始:6 0 0
n转:x 0.5x x
n平:6-x 0.5x x
即: 2 2 4
从图知C点时NO2的物质的量为2,则6-x=2,解得x=4,
则C点NO2的转化率![]() ×100%= 66.7%
×100%= 66.7%
则平衡时总的物质的量为8mol,C点时该反应的压强平衡常数Kp(C)=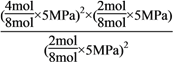 =5MPa;
=5MPa;
(5)平衡常数K=![]() =
=![]()
![]() =0.40,故答案为:0.40;
=0.40,故答案为:0.40;
(6)利用水煤气合成二甲醚的三步反应如下:①2H2(g) + CO(g) ![]() CH3OH(g); ΔH1②CH3OH(g)
CH3OH(g); ΔH1②CH3OH(g) ![]() CH2OCH3(g) + H2O(g); ΔH2③CO(g) + H2O(g)
CH2OCH3(g) + H2O(g); ΔH2③CO(g) + H2O(g) ![]() CO2(g) + H2(g); ΔH3,由盖斯定律,①×2+②+③得总反应: 3H2(g)+3CO(g)
CO2(g) + H2(g); ΔH3,由盖斯定律,①×2+②+③得总反应: 3H2(g)+3CO(g) ![]() CH2OCH3(g)+CO2(g)的ΔH=2ΔH1+ΔH2+ΔH3。
CH2OCH3(g)+CO2(g)的ΔH=2ΔH1+ΔH2+ΔH3。

【题目】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,合成氨工业在国民生产中有重要意义。以下是关于合成氨的有关问题,请回答:
(1)若在一容积为2 L的密闭容器中加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生反应: N2(g) +3H2(g)![]() 2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2 mol。则前5分钟的平均反应速率v(N2)=________。
2NH3(g) ΔH<0,若在5分钟时反应达到平衡,此时测得NH3的物质的量为0.2 mol。则前5分钟的平均反应速率v(N2)=________。
(2)平衡后,若要提高H2的转化率,可以采取的措施有________。
A.加了催化剂 B.增大容器体积 C.降低反应体系的温度 D.加入一定量N2
(3)若在0.5 L的密闭容器中,一定量的氮气和氢气进行如下反应:N2(g)+3H2(g)![]() 2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示:
2NH3(g) ΔH<0,其化学平衡常数K与温度T的关系如表所示:
T/℃ | 200 | 300 | 400 |
K | K1 | K3 | 0.5 |
请完成下列问题:
①试比较K1、K2的大小,K1________K2(填“<”、“>”或“=”);
②下列各项能作为判断该反应达到化学平衡状态的依据是________(填序号字母)
A.容器内N2、H2、NH3的物质的量浓度之比为1∶3∶2
B.v(H2)正=3v(H2)逆
C.容器内压强保持不变
D.混合气体的密度保持不变
③400℃时,反应2NH3(g)![]() N2(g)+3H2(g)的化学平衡常数为________。当测得NH3、N2和H2物质的量分别为3 mol、2 mol和 1 mol时,则该反应的v(N2)正________v(N2)逆(填“<”、“>”或“=”)。
N2(g)+3H2(g)的化学平衡常数为________。当测得NH3、N2和H2物质的量分别为3 mol、2 mol和 1 mol时,则该反应的v(N2)正________v(N2)逆(填“<”、“>”或“=”)。
(4)根据化学反应速率和化学平衡理论,联系合成氨的生产实际,你认为下列说法不正确的是________。
A.化学反应速率理论可指导怎样在一定时间内快出产品
B.勒夏特列原理可指导怎样使用有限原料多出产品
C.催化剂的使用是提高产品产率的有效方法
D.正确利用化学反应速率和化学反应限度理论都可以提高化工生产的综合经济效益