题目内容
19.下列物质中,既有离子键又有共价键的是( )| A. | MgCl2 | B. | Ca(OH)2 | C. | H2O | D. | C60 |
分析 一般来说,活泼金属与非金属形成离子键,非金属之间形成共价键,以此来解答.
解答 解:A.氯化镁只含离子键,故A不选;
B.含离子键和O-H共价键,故B选;
C.水中只含共价键,故C不选;
D.C60为单质,只含非极性共价键,故D不选;
故选C.
点评 本题考查离子化合物及化学键,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,注意常见物质中的化学键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.铝热剂中铝的作用是( )
| A. | 催化剂 | B. | 氧化剂 | C. | 还原剂 | D. | 填充剂 |
10.下列说法不正确的是( )
| A. | 等体积等浓度的Na2S溶液和Na2SO3溶液中,离子数目以前者为多 | |
| B. | 已知室温时0.10mol/L NH4Cl溶液中c(H+)=7.5×10-6mol/L,室温时0.10mol/L KCN溶液中c (OH-)=1.3×10-3mol/L.那么此时0.10mol/L NH4CN溶液中pH>7 | |
| C. | 等pH、等体积的醋酸和硫酸,分别与足量的碳酸氢钠反应,在相同条件下,硫酸放出气体更多 | |
| D. | 醋酸加到氢氧化钠溶液中,若要使所得溶液呈中性,醋酸应稍过量 |
7.下列叙述正确的是( )
| A. | 核素就是同位素 | |
| B. | 元素的金属性强弱与元素失去电子数的多少成正比 | |
| C. | 具有相同质子数的微粒一定是同一种元素 | |
| D. | 核内中子数为N的R2+,质量数为A,则该离子的核外电子数为A-N-2 |
14.下列各组物质中,互为同位素的是( )
| A. | T2O与D2O | B. | 4019K与4020C | C. | O2和O3 | D. | 21H和31H |
4.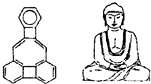 美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛.有关该有机分子的说法正确的是( )
美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛.有关该有机分子的说法正确的是( )
 美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛.有关该有机分子的说法正确的是( )
美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛.有关该有机分子的说法正确的是( )| A. | 该有机物属于芳香烃 | B. | 该有机物属于苯的同系物 | ||
| C. | 该有机物分子中含有23个碳原子 | D. | 该有机物的一氯代物有3种 |
11.乙醇的结构式如下所示,关于乙醇性质的说法正确的是( )
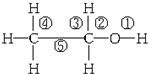

| A. | 乙醇与金属钠、乙酸、HBr的反应均是①处化学键断裂 | |
| B. | 乙醇燃烧时,①②③④⑤处化学键全部断裂 | |
| C. | 乙醇与浓硫酸170℃时反应,①③处化学键断裂 | |
| D. | 乙醇与氧化铜加热反应,①②③④⑤处化学键全部断裂 |
9.下列有关实验原理、方法和结论都正确的是( )
| A. | 滴加盐酸酸化的BaCl2溶液,生成白色沉淀,原溶液中一定含有SO42- | |
| B. | 将钾盐溶于盐酸,产生能使澄清石灰水变浑浊的气体,该钾盐一定为K2C03 | |
| C. | 某固体进行焰色反应实验,火焰呈黄色,说明该固体为钠盐 | |
| D. | 向某溶液中滴加KSCN溶液,不变色,再滴加氯水显红色,则 溶液中一定含有Fe2+ |
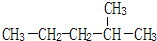 2-甲基戊烷
2-甲基戊烷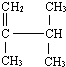 2,3-二甲基-1-丁烯
2,3-二甲基-1-丁烯 1,2-二溴乙烷
1,2-二溴乙烷 乙苯
乙苯