题目内容
【题目】已知:乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,1570C时开始分解:
(1)探究草酸的酸性
250C H2C2O4 K1 = 5.4 x 10-2,K2 = 5. 4 x 10 -5 ;H2CO3 K1=4.5x10-7 K2= 4.7X10-11
下列化学方程式可能正确的是________
A. H2C2O4 +CO32-=HCO3- +HC2O4- B. HC2O4- +CO32-= HCO3-+C2O42-
C. 2C2O42-+CO2+H2O=2HC2O4-+CO32- D. H2C2O4 +CO32-=C2O42-+H2O+CO2
(2)探究草酸分解产物
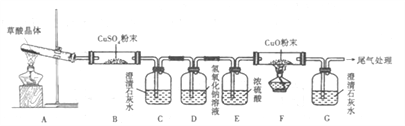
①实验中观察到B中CuSO4粉末变蓝,C中澄清石灰水变浑浊,D的作用:_______,证明有CO气体生成的现象是:_____________________
②写出H2C2O4分解的化学方程式_____________________
(3)探究催化剂对化学反应速率的影响
在甲、乙两支试管中各加人4mLO.O1mol/T. KMnO4酸性溶液和2mL O.1mol/L H2C2O4溶液, 再向乙试管中加人一粒黄豆大的MnSO4固体,摇匀。填写下表:
反应现象 | ______________ |
实验结论 | ______________ |
试管中发送反应的离子方程式 | ______________ |
(4)用酸性KMnO4溶液滴定Na2C2O4求算Na2C2O4的纯度
实验步骤:准确称取2.OgNa2C2O4固体,配成1OO mL溶液,取出20.OOmL于锥形瓶中=再向瓶 中加人足量稀H2SO4 ,用0.0160mol/L酸性高锰酸钾溶液滴定,滴定至终点时消耗高锰酸钾溶液25.OOmL0
①高锰酸钾溶液应装在_______滴定管中。(填“酸 式”或“碱 式”)
②滴定至终点时的实验现象是:______________。
③Na2C2O4的纯度是:______________
【答案】 BD 吸收二氧化碳气体, F中黑色变红色,G中澄清石灰水变混浊 H2C2O4![]() CO2↑+CO↑+H2O↑ 两只试管中紫色高锰酸钾溶液均褪色,乙试管褪色较快; 硫酸锰是催化剂,加入催化剂速率加快; 2MnO4-+5H2C2O4+6H+=10CO2↑+2Mn2++8H2O 酸式; 滴入最后一滴高锰酸钾,溶液由无色变为紫色,且半分钟内不褪色; 【答题空10】33.5%
CO2↑+CO↑+H2O↑ 两只试管中紫色高锰酸钾溶液均褪色,乙试管褪色较快; 硫酸锰是催化剂,加入催化剂速率加快; 2MnO4-+5H2C2O4+6H+=10CO2↑+2Mn2++8H2O 酸式; 滴入最后一滴高锰酸钾,溶液由无色变为紫色,且半分钟内不褪色; 【答题空10】33.5%
【解析】(1)根据电离平衡常数可知酸性强弱顺序是:H2C2O4>HC2O4->H2CO3>HCO3-,根据强酸制取弱酸知草酸和碳酸根离子反应生成草酸根离子和二氧化碳,草酸氢根离子和碳酸根离子反应生成碳酸氢根离子和草酸根离子,答案选BD;(2)①氢氧化钠是强碱能吸收酸性氧化物二氧化碳,故D的作用是:吸收CO2气体;一氧化碳具有还原性,能还原黑色的氧化铜生成红色的铜,同时自身被氧化生成二氧化碳,二氧化碳使澄清的石灰水变浑浊,所以看到的现象是:F中黑色CuO变成光亮的红色,G中澄清石灰水变浑浊;②该反应中反应物是草酸,生成物是水、二氧化碳和一氧化碳,反应条件是加热,所以该反应方程式为H2C2O4![]() CO2↑+CO↑+H2O↑;(3)看到的现象是两支试管中紫色KMnO4溶液均褪色,乙试管中溶液褪色较快;通过对比实验知,硫酸锰是该反应的催化剂,加入催化剂能加快反应速率;该反应中高锰酸根离子被还原生成锰离子,草酸被氧化生成二氧化碳,离子反应方程式为:2MnO4-+5H2C2O4+6H+=10CO2↑+2Mn2++8H2O;(4)①高锰酸钾溶液呈酸性,应该用酸式滴定管量取; ②当入最后一滴KMnO4,高锰酸钾溶液过量,溶液由无色变为紫色;③设草酸钠的质量分数为x,
CO2↑+CO↑+H2O↑;(3)看到的现象是两支试管中紫色KMnO4溶液均褪色,乙试管中溶液褪色较快;通过对比实验知,硫酸锰是该反应的催化剂,加入催化剂能加快反应速率;该反应中高锰酸根离子被还原生成锰离子,草酸被氧化生成二氧化碳,离子反应方程式为:2MnO4-+5H2C2O4+6H+=10CO2↑+2Mn2++8H2O;(4)①高锰酸钾溶液呈酸性,应该用酸式滴定管量取; ②当入最后一滴KMnO4,高锰酸钾溶液过量,溶液由无色变为紫色;③设草酸钠的质量分数为x,
2MnO4- + 5H2C2O4 + 6H+=10CO2↑+2Mn2++8H2O
2 5
0.0160mol/L×0.025L (![]() )mol
)mol
x=![]() ×100%=33.5%。
×100%=33.5%。

【题目】利用如图所示装置测定中和热的实验步骤如下:
①用量筒量取50 mL 0.50 mol·L-1盐酸倒入小烧杯中,测出盐酸温度;②用另一量筒量取50 mL 0.55 mol·L-1NaOH溶液,并用另一温度计测出其温度;③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液温度。
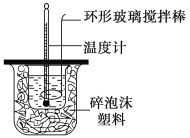
回答下列问题:
(1)倒入NaOH溶液的正确操作是________(填序号)。
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(2)使盐酸与NaOH溶液混合均匀的正确操作是________(填序号)。
A.用温度计小心搅拌
B.揭开泡沫塑料板用玻璃棒搅拌
C.轻轻地振荡烧杯
D.用套在温度计上的环形玻璃搅拌棒轻轻地上下搅动
(3)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1 L 1 mol·L-1的稀盐酸恰好完全反应,其反应热分别为ΔH1、ΔH2、ΔH3,则ΔH1、ΔH2、ΔH3的大小关系为__________________。
(4)假设盐酸和氢氧化钠溶液的密度都是1 g·cm-3,又知中和反应后生成溶液的比热容c=4.18 J·g-1·℃-1。为了计算中和热,某学生记录数据如下:
实验序号 | 起始温度t1/ ℃ | 终止温度t2/ ℃ | |
盐酸 | 氢氧化钠溶液 | 混合溶液 | |
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |
依据该学生的实验数据计算,该实验测得的中和热ΔH=________(结果保留一位小数)。
(5)________(填“能”或“不能”)用Ba(OH)2溶液和硫酸代替氢氧化钠溶液和盐酸,理由是____________________________________________________。