题目内容
【题目】实验室用下图装置制取少量溴苯,试填写下列空白。

(1)请写出仪器名称,a__________、 d __________,在烧瓶a中装的试是__________、__________、_________。
(2)请你推测长直导管b的作用:一是_____________________________,二是____________________________________的作用。
(3)请你分析导管c的下口可否浸没于液面中?为什么?____________________________________
(4)反应完毕后,向锥形瓶d中滴加AgNO3溶液有________生成,此现象说明这种获得溴苯的反应属于:____________________。(填有机反应类型)
(5)课本采用如下装置进行实验,请在图中标出冷凝水流动方向______(上或下)口进________(上或下)口出。

【答案】 圆底烧瓶 锥形瓶 苯 Br2 铁粉 导气 冷凝和回流 不能,因为HBr易溶于水,造成倒吸 淡黄色沉淀 取代反应 下 上
【解析】(1)根据装置图,仪器a为圆底烧瓶,d为锥形瓶,苯和液溴在铁的作用下生成溴苯和HBr,故答案为:圆底烧瓶;锥形瓶;苯;溴;铁粉;
(2)苯与液溴发生取代反应,生成溴苯和HBr,由于反应放热,溴、苯沸点低,易挥发,所以从导管导出的气体中可能含有一定的溴和苯.故长导管的作用为导气兼冷凝、回流反应物,故答案为:导气;冷凝和回流;
(3)HBr极易溶于水,不能将导管c末端浸没于液面中,导管c末端与锥形瓶里液面保持一段距离的目的是防倒吸,故答案为:不能,因为HBr易溶于水,容易造成倒吸;
(4)反应完毕,锥形瓶d中是氢溴酸的容易,滴加AgNO3溶液有淡黄色溴化银沉淀生成,此现象说明反应是生成了溴化氢,说明该反应属于取代反应,故答案为:淡黄色沉淀;取代反应;
(5)冷凝水的流动方向应自下而上,可以确保冷凝管中充满冷却水,这样的冷却效果好,确保充分冷却,即冷凝水从下口进,上口出,故答案为:下;上。

【题目】已知:乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,1570C时开始分解:
(1)探究草酸的酸性
250C H2C2O4 K1 = 5.4 x 10-2,K2 = 5. 4 x 10 -5 ;H2CO3 K1=4.5x10-7 K2= 4.7X10-11
下列化学方程式可能正确的是________
A. H2C2O4 +CO32-=HCO3- +HC2O4- B. HC2O4- +CO32-= HCO3-+C2O42-
C. 2C2O42-+CO2+H2O=2HC2O4-+CO32- D. H2C2O4 +CO32-=C2O42-+H2O+CO2
(2)探究草酸分解产物
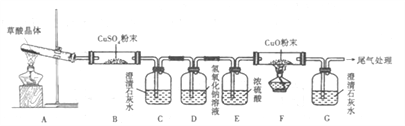
①实验中观察到B中CuSO4粉末变蓝,C中澄清石灰水变浑浊,D的作用:_______,证明有CO气体生成的现象是:_____________________
②写出H2C2O4分解的化学方程式_____________________
(3)探究催化剂对化学反应速率的影响
在甲、乙两支试管中各加人4mLO.O1mol/T. KMnO4酸性溶液和2mL O.1mol/L H2C2O4溶液, 再向乙试管中加人一粒黄豆大的MnSO4固体,摇匀。填写下表:
反应现象 | ______________ |
实验结论 | ______________ |
试管中发送反应的离子方程式 | ______________ |
(4)用酸性KMnO4溶液滴定Na2C2O4求算Na2C2O4的纯度
实验步骤:准确称取2.OgNa2C2O4固体,配成1OO mL溶液,取出20.OOmL于锥形瓶中=再向瓶 中加人足量稀H2SO4 ,用0.0160mol/L酸性高锰酸钾溶液滴定,滴定至终点时消耗高锰酸钾溶液25.OOmL0
①高锰酸钾溶液应装在_______滴定管中。(填“酸 式”或“碱 式”)
②滴定至终点时的实验现象是:______________。
③Na2C2O4的纯度是:______________
【题目】苯甲酸乙酯(![]() )(Mr=150)(密度1.05g·cm-3)稍有水果气味,用于配制香水香精和人造精油;也大量用于食品中,也可用作有机合成中间体、溶剂如纤维素酯、纤维素醚、树脂等。可能用到的数据:
)(Mr=150)(密度1.05g·cm-3)稍有水果气味,用于配制香水香精和人造精油;也大量用于食品中,也可用作有机合成中间体、溶剂如纤维素酯、纤维素醚、树脂等。可能用到的数据:
沸点(°C,1atm) | ||||||
苯甲酸 | 苯甲酸乙酯 | 石油醚 | 水 | 乙醇 | 环己烷 | 共沸物(环已烷-水-乙醇) |
249 | 212.6 | 40-80 | 100 | 78.3 | 80.75 | 62.6 |
其制备原理如下 :
制备过程:
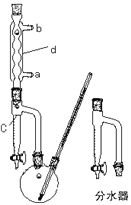
Ⅰ、制备粗产品:如右图所示的装置中,于50mL圆底烧瓶中加入8.0g苯甲酸(固体)(Mr=122)、20mL乙醇(Mr=46)、15mL环己烷、3mL浓硫酸,摇匀,加沸石。在分水器上加水至c处,接通冷凝水,水浴回流约2h,反应基本完成。记录体积,继续蒸出多余的环己烷和乙醇(从分水器中放出)。
Ⅱ、粗产品的纯化:加水30mL,分批加入固体NaHCO3。分液,水层用20mL石油醚分两次萃取。合并有机层,用无水硫酸镁干燥。回收石油醚,加热精馏,收集210-213℃馏分。
(1) 仪器d的名称__________________,水流方向为____进____出。
(2) 该反应水浴控制的温度为____________。
(3) 该反应加过量乙醇的目的为________________________________。
(4) 分水器的作用____________________,分水器的检漏方法_____________。如何利用实验现象判断反应已基本完成_______________。
(5) 固体碳酸氢钠的作用______________________,加至___________________为止。
(6) 经精馏得210-213℃馏分7.0mL,则该反应的产率为___________。