题目内容
8.化学用语是学好化学知识的重要基础,下列有关化学用语表示正确的是( )①用电子式表示HCl的形成过程:
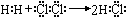 ;
;②MgCl2 的电子式:
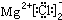 ,
,③质量数为133、中子数为78的铯原子:${\;}_{55}^{133}$Cs
④乙烯、乙酸结构简式依次为:CH2CH2、C2H4O2
⑤S2-的结构示意图:
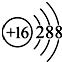
| A. | ①②③④⑤ | B. | ④⑤ | C. | ③④⑤ | D. | ③⑤ |
分析 ①用电子式表示HCl的形成过程,应该为氯原子与氢原子形成共价化合物氯化氢;
②氯化镁的电子式中,两个氯原子不能合并;
③铯的质子数为133-78=55,质量数为133;
④有机物的结构简式中需要标出其官能团;
⑤硫原子核电荷数为16,核外电子总数为18.
解答 解:①用电子式表示HCl的形成过程为: ,故①错误;
,故①错误;
②氯化镁为离子化合物,氯离子不能合并,MgCl2 的电子式为: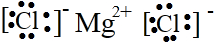 ,故②错误;
,故②错误;
③质量数为133、中子数为78的铯原子,其质子数为55,铯原子表示为:${\;}_{55}^{133}$Cs,故③正确;
④乙烯、乙酸结构简式中应该标出官能团,乙烯、乙酸的结构简式依次为:CH2═CH2、CH3COOH,故④错误;
⑤硫离子核电荷数为16,核外电子数为18,S2-的结构示意图为: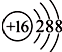 ,故⑤正确;
,故⑤正确;
故选D.
点评 本题考查了结构简式、离子结构示意图、电子式等知识,题目难度中等,注意掌握常见化学用语的表示方法,明确电子式、结构简式、结构式等概念及区别,试题培养了学生规范答题都能了.

练习册系列答案
相关题目
17.标准状况下相同质量的下列气体体积最大的是( )
| A. | O2 | B. | Cl2 | C. | N2 | D. | CO2 |
19.元素周期表中短周期的一部分如右图,关于X、Y、Z、W、Q说法正确的是( )


| A. | 元素Y与元素Z的最高正化合价之和的数值等于9 | |
| B. | 原子半径的大小顺序为:W>Z>Y | |
| C. | 离子半径的大小顺序为:W2->Y2->Z3+ | |
| D. | W的气态氢化物的热稳定性和还原性均比Q的氢化物的强 |
16.下列叙述正确的是( )
| A. | 分子式为C3H6有机物最多存在4个C-C单键,与C5H12的碳碳单键数相同 | |
| B. | 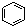 和 和  均是芳香烃, 均是芳香烃, 既是芳香烃又是芳香化合物 既是芳香烃又是芳香化合物 | |
| C. | 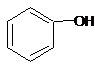 和 和 分子组成相差一个-CH2-,因此是同系物 分子组成相差一个-CH2-,因此是同系物 | |
| D. | 分子式为C2H6O的红外光谱图上发现有C-H键和C-O键的振动吸收,由此推测可能有H-O键 |
13.下列难溶盐的饱和溶液中,Ag+浓度最大的是( )
| A. | AgCl(Ksp=1.56×10-10) | B. | Ag2CO3(Ksp=8.1×10-12) | ||
| C. | Ag2CrO4(Ksp=9.0×10-12) | D. | AgBr(Ksp=5.0×10-13) |
20.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 30g二氧化硅晶体中含有Si-O键数目为2NA | |
| B. | 标准状况下,2.24L CHCl3的原子总数为0.1NA | |
| C. | 一定条件下,将1molN2与3molH2混合反应后,生成NH3分子的数目为2NA | |
| D. | 常温下,0.1mol/LNH4NO3溶液NO${\;}_{3}^{-}$的数目为0.1NA |
17.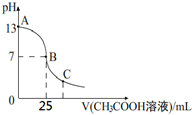 25℃时,向25mL 一定浓度的 NaOH溶液中逐滴加入某浓度的 CH3COOH溶液,溶液pH和加入的醋酸溶液的体积关系曲线如图所示.下列有关混合溶液说法错误的是( )
25℃时,向25mL 一定浓度的 NaOH溶液中逐滴加入某浓度的 CH3COOH溶液,溶液pH和加入的醋酸溶液的体积关系曲线如图所示.下列有关混合溶液说法错误的是( )
 25℃时,向25mL 一定浓度的 NaOH溶液中逐滴加入某浓度的 CH3COOH溶液,溶液pH和加入的醋酸溶液的体积关系曲线如图所示.下列有关混合溶液说法错误的是( )
25℃时,向25mL 一定浓度的 NaOH溶液中逐滴加入某浓度的 CH3COOH溶液,溶液pH和加入的醋酸溶液的体积关系曲线如图所示.下列有关混合溶液说法错误的是( )| A. | A、B间的溶液中可能有:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| B. | B点:c(CH3COO-)=c(Na+)>c(OH-)=c(H+) | |
| C. | C点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| D. | NaOH溶液和醋酸溶液的浓度都恰好为0.1 mol•L-1 |