题目内容
20.设NA为阿伏加德罗常数的值,下列叙述正确的是( )| A. | 30g二氧化硅晶体中含有Si-O键数目为2NA | |
| B. | 标准状况下,2.24L CHCl3的原子总数为0.1NA | |
| C. | 一定条件下,将1molN2与3molH2混合反应后,生成NH3分子的数目为2NA | |
| D. | 常温下,0.1mol/LNH4NO3溶液NO${\;}_{3}^{-}$的数目为0.1NA |
分析 A.二氧化硅结构中每一个硅原子形成4个Si-O键;
B.标准状况下,三氯甲烷的状态为液体,不是气体;
C.氨气与氢气生成氨气的反应为可逆反应,反应物不可能完全转化成生成物;
D.缺少溶液体积,无法计算溶液中硝酸根离子的数目.
解答 解:A.30g二氧化硅的物质的量为:$\frac{30g}{60g/mol}$=0.5mol,1mol二氧化硅中含有4mol硅氧键,则0.5mol二氧化硅中含有硅氧键的物质的量为:0.5mol×4=2mol,含有Si-O键数目为2NA,故A正确;
B.标况下三氯甲烷不是气体,不能使用标况下的气体摩尔体积计算,故B错误;
C.合成氨的反应为可逆反应,则1molN2与3molH2混合反应后生成的氨气小于2mol,生成NH3分子的数目小于2NA,故C错误;
D.没有告诉溶液体积,无法计算溶液中硝酸根离子的数目,故D错误;
故选A.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下乙醇、水、四氯化碳、三氯甲烷等物质的状态不是气体,熟练掌握以物质的量为中心的各化学量与阿伏加德罗常数的关系;D为易错点,注意题中缺少溶液体积.

练习册系列答案
相关题目
8.化学用语是学好化学知识的重要基础,下列有关化学用语表示正确的是( )
①用电子式表示HCl的形成过程: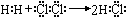 ;
;
②MgCl2 的电子式: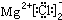 ,
,
③质量数为133、中子数为78的铯原子:${\;}_{55}^{133}$Cs
④乙烯、乙酸结构简式依次为:CH2CH2、C2H4O2
⑤S2-的结构示意图: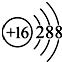
①用电子式表示HCl的形成过程:
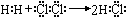 ;
;②MgCl2 的电子式:
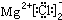 ,
,③质量数为133、中子数为78的铯原子:${\;}_{55}^{133}$Cs
④乙烯、乙酸结构简式依次为:CH2CH2、C2H4O2
⑤S2-的结构示意图:
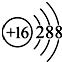
| A. | ①②③④⑤ | B. | ④⑤ | C. | ③④⑤ | D. | ③⑤ |
15.不粘锅是在普通锅的内侧涂覆上一层树脂而成,这层树脂的主要成分是聚四氟乙烯.洗衣店干洗西装是用有机溶剂来洗衣服的,目前使用的标准干洗剂的主要成分是四氯乙烯.关于聚四氟乙烯和四氯乙烯,下面的说法正确的是( )
| A. | 它们都是乙烯的同系物 | B. | 它们都属于混合物 | ||
| C. | 它们的分子中都含有C=C双键 | D. | 它们分子中都不含氢原子 |
5.下列化学式中,能真实表示物质的分子组成的是( )
| A. | CuSO4 | B. | CS2 | C. | Ar | D. | CsCl |
12.下列说法正确的是( )
| A. | 凡金属跟非金属元素化合时都能形成离子键 | |
| B. | 离子化合物熔融状态下一定导电 | |
| C. | 离子化合物中的阳离子只能是金属离子,酸根离子中不能含有金属元素 | |
| D. | 溶于水可以导电的化合物一定是离子化合物 |
9.下面几组物质,请将合适组号填写在下表中.
①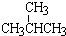 和
和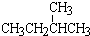 ; ②
; ②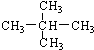 和
和 ; ③CH4和CH3CH2CH3;④金刚石与石墨;⑤氕、氘与氚;⑥16O、17O和18O;⑦乙醇(CH3CH2OH)和二甲醚(CH3OCH3);⑧氧气(O2)与臭氧(O3).
; ③CH4和CH3CH2CH3;④金刚石与石墨;⑤氕、氘与氚;⑥16O、17O和18O;⑦乙醇(CH3CH2OH)和二甲醚(CH3OCH3);⑧氧气(O2)与臭氧(O3).
①
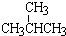 和
和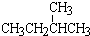 ; ②
; ②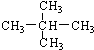 和
和 ; ③CH4和CH3CH2CH3;④金刚石与石墨;⑤氕、氘与氚;⑥16O、17O和18O;⑦乙醇(CH3CH2OH)和二甲醚(CH3OCH3);⑧氧气(O2)与臭氧(O3).
; ③CH4和CH3CH2CH3;④金刚石与石墨;⑤氕、氘与氚;⑥16O、17O和18O;⑦乙醇(CH3CH2OH)和二甲醚(CH3OCH3);⑧氧气(O2)与臭氧(O3).| 类别 | 同位素 | 同系物 | 同素异形体 | 同分异构体 |
| 组号 | ⑤⑥ | ①③ | ④⑧ | ②⑦ |
10.下列有关说法错误的是( )
| A. | 已知氯化钴及其水合物会呈现不同颜色(如下),德国科学家发明了添加氯化钴的变色水泥,据此推测雨天变色水泥呈粉红色 | |
| B. | 已知铬酸根(黄色)和重铬酸根(橙色)离子间存在如下平衡:2CrO42-+2H+?Cr2O72-+H2O,若加水稀释,则溶液中所有离子浓度均减少 | |
| C. | 若反应2A(g)+B(s)?C(g)+3D(g)只有高温下才能自发进行,则该反应的△H>0 | |
| D. | 增大反应物的浓度,可使单位体积内活化分子数目增多,反应速率加快 |