题目内容
17.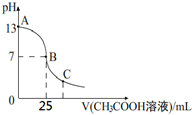 25℃时,向25mL 一定浓度的 NaOH溶液中逐滴加入某浓度的 CH3COOH溶液,溶液pH和加入的醋酸溶液的体积关系曲线如图所示.下列有关混合溶液说法错误的是( )
25℃时,向25mL 一定浓度的 NaOH溶液中逐滴加入某浓度的 CH3COOH溶液,溶液pH和加入的醋酸溶液的体积关系曲线如图所示.下列有关混合溶液说法错误的是( )| A. | A、B间的溶液中可能有:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| B. | B点:c(CH3COO-)=c(Na+)>c(OH-)=c(H+) | |
| C. | C点:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| D. | NaOH溶液和醋酸溶液的浓度都恰好为0.1 mol•L-1 |
分析 25℃时,向25mL一定浓度的 NaOH溶液中逐滴加入某浓度的 CH3COOH溶液,二者恰好中和时溶质为CH3COONa溶液,溶液呈碱性,而图象中25mL NaOH溶液的pH为13,则NaOH的浓度为0.1 mol•L-1;向其中加入25mL CH3COOH溶液时溶液的pH=7,呈中性,说明此时酸稍过量,即酸的浓度应大于0.1 mol•L-1;然后结合电荷守恒、盐的水解原理对各选项进行判断.
解答 解:A.当氢氧化钠和醋酸恰好反应时,溶质为醋酸钠,溶液呈碱性,应该处于A、B之间,此时溶液中离子浓度大小为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故A正确;
B.B点时溶液的pH=7,溶液为中性,则c(OH-)=c(H+),根据电荷守恒可知:c(CH3COO-)=c(Na+),则溶液中离子浓度大小为:c(CH3COO-)=c(Na+)>c(OH-)=c(H+),故B正确;
C.C点时溶液呈酸性,则:c(H+)>c(OH-),结合电荷守恒可知:c(CH3COO-)>c(Na+),溶液中离子浓度大小为:c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故C正确;
D.图象中25mL NaOH溶液的pH为13,则NaOH的浓度为0.1 mol•L-1,向其中加入25mL CH3COOH溶液时溶液的pH=7,呈中性,说明此时酸稍过量,即酸的浓度应大于0.1 mol•L-1,故D错误;
故选D.
点评 本题考查了酸碱混合的定性判断及溶液pH的计算,题目难度中等,明确图象中各点溶质组成为解答关键,注意掌握溶液酸碱性与溶液pH的关系及计算方法,能够根据电荷守恒、物料守恒及盐的水解原理判断各离子浓度大小.

练习册系列答案
相关题目
7.下列有关化学用语使用不正确的是( )
| A. | 原子核内有l8个中子的氯原子:${\;}_{17}^{35}$Cl | |
| B. | S2-的结构示意图: | |
| C. | CO2分子比例模型: | |
| D. | H2O2的电子式: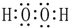 |
8.化学用语是学好化学知识的重要基础,下列有关化学用语表示正确的是( )
①用电子式表示HCl的形成过程: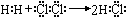 ;
;
②MgCl2 的电子式: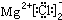 ,
,
③质量数为133、中子数为78的铯原子:${\;}_{55}^{133}$Cs
④乙烯、乙酸结构简式依次为:CH2CH2、C2H4O2
⑤S2-的结构示意图: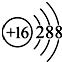
①用电子式表示HCl的形成过程:
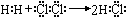 ;
;②MgCl2 的电子式:
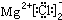 ,
,③质量数为133、中子数为78的铯原子:${\;}_{55}^{133}$Cs
④乙烯、乙酸结构简式依次为:CH2CH2、C2H4O2
⑤S2-的结构示意图:
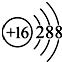
| A. | ①②③④⑤ | B. | ④⑤ | C. | ③④⑤ | D. | ③⑤ |
5.下列化学式中,能真实表示物质的分子组成的是( )
| A. | CuSO4 | B. | CS2 | C. | Ar | D. | CsCl |
12.下列说法正确的是( )
| A. | 凡金属跟非金属元素化合时都能形成离子键 | |
| B. | 离子化合物熔融状态下一定导电 | |
| C. | 离子化合物中的阳离子只能是金属离子,酸根离子中不能含有金属元素 | |
| D. | 溶于水可以导电的化合物一定是离子化合物 |
9.下面几组物质,请将合适组号填写在下表中.
①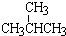 和
和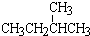 ; ②
; ②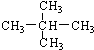 和
和 ; ③CH4和CH3CH2CH3;④金刚石与石墨;⑤氕、氘与氚;⑥16O、17O和18O;⑦乙醇(CH3CH2OH)和二甲醚(CH3OCH3);⑧氧气(O2)与臭氧(O3).
; ③CH4和CH3CH2CH3;④金刚石与石墨;⑤氕、氘与氚;⑥16O、17O和18O;⑦乙醇(CH3CH2OH)和二甲醚(CH3OCH3);⑧氧气(O2)与臭氧(O3).
①
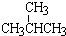 和
和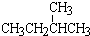 ; ②
; ②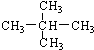 和
和 ; ③CH4和CH3CH2CH3;④金刚石与石墨;⑤氕、氘与氚;⑥16O、17O和18O;⑦乙醇(CH3CH2OH)和二甲醚(CH3OCH3);⑧氧气(O2)与臭氧(O3).
; ③CH4和CH3CH2CH3;④金刚石与石墨;⑤氕、氘与氚;⑥16O、17O和18O;⑦乙醇(CH3CH2OH)和二甲醚(CH3OCH3);⑧氧气(O2)与臭氧(O3).| 类别 | 同位素 | 同系物 | 同素异形体 | 同分异构体 |
| 组号 | ⑤⑥ | ①③ | ④⑧ | ②⑦ |
6.我国有丰富的天然气资源.以天然气为原料合成尿素的主要步骤如图所示(图中某些转化步骤及生成物未列出):

(1)“造合成气”发生的热化学方程式是CH4(g)+H2O(g)?CO(g)+3H2(g);△H>0在恒温恒容的条件下,欲提高CH4的反应速率和转化率,下列措施可行的是BD.
A、增大压强 B、升高温度 C、充入He气 D、增大水蒸气浓度
(2)“转化一氧化碳”发生的方程式是H2O(g)+CO(g)?H2(g)+CO2(g),该反应平衡常数随温度的
变化如下:
提高氢碳比[$\frac{n({H}_{2}O)}{n(CO)}$],K值不变(填“增大”、“不变”或“减小”);若该反应在400℃时进行,起始通入等物质的量的H2O和CO,反应进行到某一时刻时CO和CO2的浓度比为1:3,此时v(正)>v(逆)(填“>”、“=”或“<”).
(3)有关合成氨工业的说法中正确的是A.
A、该反应属于人工固氮
B、合成氨工业中使用催化剂能提高反应物的利用率
C、合成氨反应温度控制在500℃左右,目的是使化学平衡向正反应方向移动
D、合成氨工业采用循环操作的主要原因是为了加快反应速率
(4)生产尿素过程中,理论上n(NH3):n(CO2)的最佳配比为2:1,而实际生产过程中,往往使n(NH3):n(CO2)≥3,这是因为有利于提高CO2的转化率,因为NH3极易溶于水,便于分离、回收利用.
(5)当甲烷合成氨气的转化率为60%时,以3.0×108L甲烷为原料能够合成4.8×108L 氨气.(假设体积均在标准状况下测定)

(1)“造合成气”发生的热化学方程式是CH4(g)+H2O(g)?CO(g)+3H2(g);△H>0在恒温恒容的条件下,欲提高CH4的反应速率和转化率,下列措施可行的是BD.
A、增大压强 B、升高温度 C、充入He气 D、增大水蒸气浓度
(2)“转化一氧化碳”发生的方程式是H2O(g)+CO(g)?H2(g)+CO2(g),该反应平衡常数随温度的
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
提高氢碳比[$\frac{n({H}_{2}O)}{n(CO)}$],K值不变(填“增大”、“不变”或“减小”);若该反应在400℃时进行,起始通入等物质的量的H2O和CO,反应进行到某一时刻时CO和CO2的浓度比为1:3,此时v(正)>v(逆)(填“>”、“=”或“<”).
(3)有关合成氨工业的说法中正确的是A.
A、该反应属于人工固氮
B、合成氨工业中使用催化剂能提高反应物的利用率
C、合成氨反应温度控制在500℃左右,目的是使化学平衡向正反应方向移动
D、合成氨工业采用循环操作的主要原因是为了加快反应速率
(4)生产尿素过程中,理论上n(NH3):n(CO2)的最佳配比为2:1,而实际生产过程中,往往使n(NH3):n(CO2)≥3,这是因为有利于提高CO2的转化率,因为NH3极易溶于水,便于分离、回收利用.
(5)当甲烷合成氨气的转化率为60%时,以3.0×108L甲烷为原料能够合成4.8×108L 氨气.(假设体积均在标准状况下测定)
7.下列化学用语表述正确的是( )
| A. | 羟基的电子式: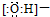 | B. | 硫原子的原子结构示意图: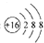 | ||
| C. | 乙烯分子的实验式:C2H4 | D. | 3,3一二甲基一1一戊烯的键线式: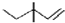 |