题目内容
14. 依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题:
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.请回答下列问题:(1)电极X的材料是Cu;电解质溶液Y是AgNO3 ;
(2)银电极为电池的正极,发生的电极反应式为Ag++e-=Ag;X电极上发生的电极反应为氧化反应反应;(填“氧化”或“还原”)
(3)外电路中的电子流向(填“流出”或“流向”)Ag电极.
(4)当有1.6g铜溶解时,银棒增重5.4 g.
分析 (1)根据电池反应式知,失电子化合价升高的金属作负极,不如负极活泼的金属或导电的非金属作正极,得电子的化合价降低的可溶性反应物作电解质溶液,据此设计原电池;
(2)原电池中,易失电子的电极铜为负极,银作正极,正极上得电子发生还原反应;负极发生氧化反应;
(3)电子从负极沿导线流向正极;
(4)根据总的电极反应式得:Cu~~2Ag.
解答 解:(1)由反应“2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)”可知,在反应中,Cu被氧化,失电子,应为原电池的负极,所以X电极材料是Cu,Ag+在正极上得电子被还原,电解质溶液为AgNO3 ,
故答案为:Cu;AgNO3 ;
(2)正极为活泼性较Cu弱的Ag,Ag+在正极上得电子被还原,电极反应为Ag++e=Ag,X电极是铜电极发生氧化反应生成铜离子,
故答案为:正; Ag++e-=Ag;氧化反应;
(3)电子从负极Cu沿导线流向正极Ag,故答案为:流向;
(4)根据总的电极反应式得:
Cu~~~~~2Ag
64g 216g
1.6g m
所以$\frac{64g}{1.6g}=\frac{216g}{m}$,解之得m=5.4g,故答案为:5.4.
点评 本题考查了原电池设计,明确原电池原理是解本题关键,根据电池反应式中得失电子的物质选取负极材料和电解质,知道原电池中正负极的判断方法,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.银锌纽扣电池放电时的反应为Zn+Ag2O═ZnO+2Ag,该电池的负极是( )
| A. | Zn | B. | Ag2O | C. | ZnO | D. | Ag |
5.下列物质不能用单质与氯气直接反应得到的物质是( )
| A. | CuCl2 | B. | FeCl2 | C. | HCl | D. | AlCl3 |
2.一定量的铝与过量的稀盐酸反应时,为了加快反应速率,但又不影响生成的氢气总量,可以采取的措施是( )
| A. | 升高温度 | B. | 加入适量的水 | ||
| C. | 加入少量CuSO4溶液 | D. | 加入浓度较大的盐酸 |
9.已知:25℃时,Ksp(Mg(OH)2)=5.61×10-12,Ksp(MgF2)=7.42×10-11.下列说法正确的是( )
| A. | 25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者的c(Mg2+)大 | |
| B. | 25℃时,Mg(OH)2固体在20 ml 0.01 mol/L氨水中的Ksp比在20 mL 0.01 mol/L NH4Cl溶液中的小 | |
| C. | 25℃时,在Mg(OH)2的悬浊液加入NaF溶液后,Mg(OH)2不可能转化成为MgF2 | |
| D. | 25℃时,在Mg(OH)2的悬浊液加入少量的NH4Cl固体,c(Mg2+)增大 |
19.图所示装置中,已知电子由b极沿导线流向锌.下列判断正确的是( )
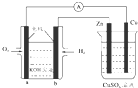

| A. | 该装置中Zn极为阳极 | |
| B. | 一段时间后铜片上质量增加 | |
| C. | a极反应的电极反应式为:O2+4e-+2H2O═4OH- | |
| D. | 当铜极的质量变化为32g时,b极上消耗的O2的体积为11.2 L |
6.在2L密闭容器中,发生3A+B=2C (均为气体)的反应,若最初加入A和B都是4mol,A的平均反应速率是0.12mol/(L.s),则10s后容器中的B的物质的量是( )
| A. | 1.6mol | B. | 3.2mol | C. | 3.6mol | D. | 2.8mol |
4.下列有关实验的叙述,正确的是( )
| A. | 用分液漏斗分离环己烷和水的混合液体 | |
| B. | 用浓氨水洗涤做过银镜反应的试管 | |
| C. | 分馏石油时,温度计的末端必须插入液面下 | |
| D. | 配制新制Cu(OH)2溶液时,在2mL10% CuSO4溶液中滴入几滴2%NaOH溶液 |
 某化学兴趣小组用如图所示装置进行电化学原理的实验探究,试回答下列问题:
某化学兴趣小组用如图所示装置进行电化学原理的实验探究,试回答下列问题: