题目内容
15.25℃时,在10mL浓度均为0.1mol•L-1的NaOH和NH3•H2O混合溶液中滴加0.1mol•L-1盐酸,下列有关溶液中粒子浓度关系正确的是( )| A. | 未加盐酸时:c(OH-)>c(Na+)=c(NH3•H2O) | B. | 加入10mL盐酸时:c(NH4+)+c(H+)=c(OH-) | ||
| C. | 加入盐酸至溶液pH=7时:c(Cl-)=c(Na+) | D. | 加入20mL盐酸时:c(Cl-)=c(NH4+)+c(Na+) |
分析 氢氧化钠为强碱,在水溶液中完全电离,一水合氨为弱碱,在水溶液中部分电离,相同体积与浓度的氢氧化钠与一水合氨其中和能力是相同的,据此分析解答即可.
解答 解:A、NaOH和NH3•H2O混合溶液中,NaOH完全电离,NH3•H2O部分电离,因此c(OH-)>0.1mol/L,c(Na+)=0.1mol/L,c(NH3•H2O)<0.1mol/L,故c(OH-)>c(Na+)>c(NH3•H2O),故A错误;
B、在此混合溶液中加入10mL盐酸,存在电中性原则:c(NH4+)+c(H+)+c(Na+)=c(OH-)+c(Cl-),由于等体积等浓度混合,故c(Na+)=c(Cl-),即c(NH4+)+c(H+)=c(OH-),故B正确;
C、加入盐酸至pH=7时,溶液呈中性,即c(H+)=c(OH-),那么c(NH4+)+c(Na+)=c(Cl-),即c(Cl-)>c(Na+),故C错误;
D、加入20mL盐酸时,此时溶液恰好为氯化钠与氯化铵的混合溶液,此时溶液呈酸性,即存在c(H+)>c(OH-),那么c(NH4+)+c(Na+)<c(Cl-),故D错误,故选B.
点评 本题主要考查酸碱混合的定性判断,题目难度中等,本题注意把握弱电解质的电离特点,易错点为C,注意酸碱中和滴定的实验原理.

练习册系列答案
相关题目
5.下列各组物质中,肯定是同系物的是( )
| A. |  和 和 | B. | CH2=CH2和 | ||
| C. | C2H2和C4H6 | D. | 正戊烷和2-甲基丁烷 |
6. 常温下,向20mL 0.1mol•L-1 CH3COOH溶液中加入0.1mol•L-1 NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中错误的是( )
常温下,向20mL 0.1mol•L-1 CH3COOH溶液中加入0.1mol•L-1 NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中错误的是( )
 常温下,向20mL 0.1mol•L-1 CH3COOH溶液中加入0.1mol•L-1 NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中错误的是( )
常温下,向20mL 0.1mol•L-1 CH3COOH溶液中加入0.1mol•L-1 NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中错误的是( )| A. | a和b之间的溶液中只存在:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| B. | b与c之间的溶液中不存在:c(CH3COO-)>c(H+)>c(Na+)>c(OH-) | |
| C. | c点时,V(NaOH溶液)<20mL,且c(CH3COO-)=c(Na+) | |
| D. | a、b、c点表示的溶液中$\frac{c(C{H}_{3}CO{O}^{-})•c({H}^{+})}{c(C{H}_{3}COOH)}$均相等 |
3.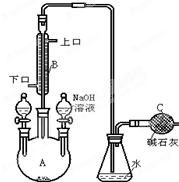 制备一溴异丙苯的实验装置如图所示,下列操作正确的是( )
制备一溴异丙苯的实验装置如图所示,下列操作正确的是( )
 制备一溴异丙苯的实验装置如图所示,下列操作正确的是( )
制备一溴异丙苯的实验装置如图所示,下列操作正确的是( )| A. | 装在左侧分液漏斗中的药品是苯和液溴 | |
| B. | 右侧分液漏斗中的物质的作用是催化剂 | |
| C. | 可向锥形瓶中加入硝酸酸化的AgNO3溶液,有淡黄色沉淀产生,说明此反应为取代反应 | |
| D. | 可在B与锥形瓶之间连接一个 装置并加入CCl4液体来除去HBr中溴蒸气 装置并加入CCl4液体来除去HBr中溴蒸气 |
10.下列有机物的命名中,正确的是( )
| A. | 1-甲基丙烷 | B. | 2-乙基丁烷 | C. | 3,3-二甲基丁烷 | D. | 2-甲基丁烷 |
2.下列各组物质的晶体,化学键类型相同,晶体类型也相同的是( )
| A. | SO2和SiO2 | B. | CO2 和NaCl | C. | NH4Cl 和HCl | D. | H2O2和C3H6 |
19.除去乙烷中混有少量乙烯的方法正确的是( )
| A. | 通入水中 | B. | 通入澄清石灰水中 | ||
| C. | 通入溴水 | D. | 混入氢气进行光照 |
20.下列溶液混合后,pH值最大的是( )
| A. | 0.1mol/LH2SO4与0.2mol/L 氨水各50mL | |
| B. | 0.1mol/LCH3COOH与0.1mol/LNaOH 溶液各50mL | |
| C. | pH=1的CH3COOH与pH=13的 NaOH 溶液各50mL | |
| D. | pH=1的盐酸与 pH=13的 NaOH 溶液各50mL |