题目内容
8.下列原子序数对应的元素间易形成共价键的是( )| A. | 11和17 | B. | 19和9 | C. | 13和17 | D. | 20和8 |
分析 由原子序数确定元素,一般来说,活泼金属元素与非金属元素形成离子键,非金属元素之间形成共价键,以此来解答.
解答 解:A.分别为Na、Cl,二者形成离子键,故A不选;
B.分别为K、F,二者形成离子键,故B不选;
C.分别为Al、Cl,二者形成共价键,故C选;
D.分别为Ca、O,二者形成离子键,故D不选;
故选C.
点评 本题考查化学键,为高频考点,把握化学键的形成、判断的一般规律及常见物质中的化学键为解答的关键,侧重分析与应用能力的考查,注意氯化铝为共价化合物这一特列,题目难度不大.

练习册系列答案
相关题目
19.某有机物的氧化产物甲和还原产物乙都能与金属钠反应放出H2,甲、乙反应可生成丙,甲、丙都能发生银镜反应,此有机物是( )
| A. | 甲醛 | B. | 乙醛 | C. | 甲酸 | D. | 乙酸 |
16. 汽车排放的尾气为大气污染源之一,目前,可利用以下化学原理解决尾气:
汽车排放的尾气为大气污染源之一,目前,可利用以下化学原理解决尾气:
2NO+2CO$\stackrel{催化剂}{?}$2CO2+N2.
(1)已知2molNO完全转化放出akJ热量,若将2molNO 和2molCO放入容器中反应,放出0.8akJ热量,则产生N2的物质的量为0.8mol.
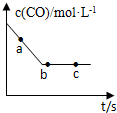
(2)一定条件下,在容积固定的容器中进行上述反应,CO浓度与时间关系如图所示:
①则反应速率υ(a)、υ(b)、υ(c)的大小关系是υ(a)>υ(b)=υ(c)
②下列可说明反应到达图中c点的是BC
A.NO、CO、CO2、N2的浓度比值保持2:2:2:1不变
B.CO的浓度不再改变
C.反应消耗2molNO的同时消耗1molN2
(3)为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究.
【资料查阅】
A.不同的催化剂对同一反应的催化效率不同;
B.使用等质量相同的催化剂时,催化剂的比表面积对催化效率有影响.
【实验设计】课题组为探究某些外界条件对汽车尾气转化反应速率的影响规律,设计了以下对比实验.
①实验编号Ⅱ的实验目的为探究催化剂比表面积对反应速率的影响.
【结论】
②由表中数据可知,升高温度,反应速率将增大.(填“增大”、“减小”、“无影响”).
 汽车排放的尾气为大气污染源之一,目前,可利用以下化学原理解决尾气:
汽车排放的尾气为大气污染源之一,目前,可利用以下化学原理解决尾气:2NO+2CO$\stackrel{催化剂}{?}$2CO2+N2.
(1)已知2molNO完全转化放出akJ热量,若将2molNO 和2molCO放入容器中反应,放出0.8akJ热量,则产生N2的物质的量为0.8mol.
(2)一定条件下,在容积固定的容器中进行上述反应,CO浓度与时间关系如图所示:
①则反应速率υ(a)、υ(b)、υ(c)的大小关系是υ(a)>υ(b)=υ(c)
②下列可说明反应到达图中c点的是BC
A.NO、CO、CO2、N2的浓度比值保持2:2:2:1不变
B.CO的浓度不再改变
C.反应消耗2molNO的同时消耗1molN2
(3)为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究.
【资料查阅】
A.不同的催化剂对同一反应的催化效率不同;
B.使用等质量相同的催化剂时,催化剂的比表面积对催化效率有影响.
【实验设计】课题组为探究某些外界条件对汽车尾气转化反应速率的影响规律,设计了以下对比实验.
| 实验编号 | 实验目的 | T/℃ | NO初始浓度 mol/L | CO初始浓度 mol/L | 同种催化剂的比表面积 m2/g | 达平衡时所用的时间min |
| Ⅰ | 参照实验 | 280 | 6.50×10-3 | 4.00×10-3 | 80 | t |
| Ⅱ | 280 | 6.50×10-3 | 4.00×10-3 | 120 | 0.5t | |
| Ⅲ | 探究温度对反应速率的影响 | 360 | 6.50×10-3 | 4.00×10-3 | 80 | 0.2t |
【结论】
②由表中数据可知,升高温度,反应速率将增大.(填“增大”、“减小”、“无影响”).
3.下列反应生成的有机物为纯净物的是( )
| A. | 甲烷和氯气光照 | B. | 氯乙烯的加聚 | ||
| C. | 溴乙烷和氢氧化钠水溶液加热 | D. | 丙烯和氯化氢加成 |
13.下列各溶液中,离子一定能大量共存的是( )
| A. | NH4+、Fe2+、NO3-、H+ | B. | K+、Mg2+、I-、ClO- | ||
| C. | K+、Ba2+、Cl-、Br- | D. | K+、HCO3-、Cl-、H+ |
20.一定温度下,在固定容积的密闭容器中发生下列反应:2HI(g)?H2(g)+I2(g).若HI浓度由0.1mol•L-1降到0.07mol•L-1时,需要15s,那么HI浓度由0.07mol•L-1降到0.05mol•L-1时,所需反应的时间为( )
| A. | 等于5 s | B. | 大于10 s | C. | 等于10 s | D. | 小于10 s |
3.CoCl2•6H2O是一种饲料营养强化剂.一种利用水钴矿[主要成分为Co2O3、Co(OH)3,还含少量Fe2O3、Al2O3、MnO等]制取CoCl2•6H2O的工艺流程如图1:
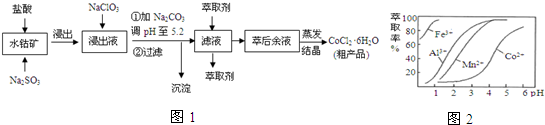
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
(1)写出浸出过程中Co2O3发生反应的离子方程式Co2O3+SO32-+4H+=2Co2++SO42-+2H2O.
(2)写出浸出液加入NaClO3发生反应的主要离子方程式ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O
(3)加Na2CO3调pH至5.2所得沉淀为Fe(OH)3、Al(OH)3.
(4)萃取剂对金属离子的萃取率与pH的关系如图2.萃取剂的作用是除去溶液中的Mn2+;其使用的较适宜pH范围是B.
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5
(5)为测定粗产品中CoCl2•6H2O含量,称取一定质 量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答一条即可)

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(2)写出浸出液加入NaClO3发生反应的主要离子方程式ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O
(3)加Na2CO3调pH至5.2所得沉淀为Fe(OH)3、Al(OH)3.
(4)萃取剂对金属离子的萃取率与pH的关系如图2.萃取剂的作用是除去溶液中的Mn2+;其使用的较适宜pH范围是B.
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5
(5)为测定粗产品中CoCl2•6H2O含量,称取一定质 量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是粗产品含有可溶性氯化物或晶体失去了部分结晶水.(答一条即可)
4.某有机物的结构简式为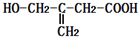 ,该有机物不可能发生的化学反应是( )
,该有机物不可能发生的化学反应是( )
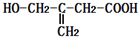 ,该有机物不可能发生的化学反应是( )
,该有机物不可能发生的化学反应是( )| A. | 还原 | B. | 水解 | C. | 氧化 | D. | 取代 |
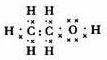 ;
;