题目内容
14.下列说法中正确的是( )| A. | 常温下pH=7的溶液中:Fe3+,Mg2+,SO42-,Cl-能大量共存 | |
| B. | 常温下水电离出c(H+)×c(OH-)=10-10的溶液中:Na+,NH4+,CH3COO-,F-不能大量共存 | |
| C. | 在含有HCO3-,HSO3-,CH3COO-,S2-四种阴离子的溶液中加入足够的Na2O2固体后,S2-浓度变化最小 | |
| D. | SO2,O2,HCl,CO2四种气体,可以大量共存于同一容器中 |
分析 A.铁离子在pH为4.4左右沉淀完全;
B.常温下水电离出c(H+)×c(OH-)=10-10的溶液,水的电离受到促进,为水解的盐溶液;
C.加入足够的Na2O2固体后,与水反应生成碱,且具有强氧化性;
D.四种气体常温下不反应.
解答 解:A.铁离子在pH为4.4左右沉淀完全,则pH=7的溶液中不能大量存在Fe3+,故A错误;
B.常温下水电离出c(H+)×c(OH-)=10-10的溶液,水的电离受到促进,为水解的盐溶液,该组离子之间不反应,可大量共存,故B错误;
C.加入足够的Na2O2固体后,与水反应生成碱,且具有强氧化性,则HSO3-、S2-均被氧化,HCO3-与碱反应,CH3COO-离子变化最小,故C错误;
D.四种气体常温下不反应,可大量共存于同一容器中,故D正确;
故选D.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
4.正确的化学实验操作对实验结果、人身安全非常重要.下图中的实验操作正确的是( )
| A. |  闻气体气味 | B. |  取用块状固体 | ||
| C. | 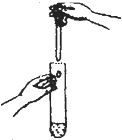 滴加液体 | D. |  稀释浓硫酸 |
5.下列物质的转化在给定条件下均能通过一步反应实现的是( )
| A. | NaAlO2(aq)$\stackrel{过量盐酸}{→}$AlCl3$\stackrel{NaOH溶液}{→}$Al2O3 | |
| B. | N2$→_{△}^{O_{2}/催化剂}$NO2$\stackrel{O_{2}、H_{2}O}{→}$HNO3 | |
| C. | NaCl(饱和)$\stackrel{NH_{3}、CO_{2}}{→}$NaHCO3$\stackrel{△}{→}$Na2CO3 | |
| D. | FeS2$\stackrel{煅烧}{→}$SO3$\stackrel{H_{2}O}{→}$H2SO4 |
19.下列关于Cl-和Cl2的说法中,正确的是( )
| A. | Cl-和Cl2均有毒 | B. | Cl-和Cl2均呈黄绿色 | ||
| C. | 相比较,Cl-稳定,Cl2活泼 | D. | Cl-和Cl2均能与金属单质反应 |
6.工业上采用电解法制备氯酸钾.电解池中的电解质是氯化钾,电解产生的Cl2与K0H混合,就得到KClO3溶液,浓缩冷却结晶即可得到氯酸钾晶体.反应原理:①2KCl+2H20$\frac{\underline{\;电解\;}}{\;}$Cl2↑+2K0H+H2↑ ②3Cl2+6K0H═KC103+5KCl+3H20.下列说法正确的是 ( )
| A. | 反应①中的K0H、Cl2和H2都是电解质 | |
| B. | 反应②属于离子反应 | |
| C. | 若反应①消耗7.45gKCl,可以制备标准状况下4.48L氯气 | |
| D. | 反应②中氧化剂和还原剂的质量之比是1:5 |

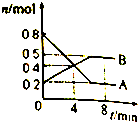 某温度时.在2L密闭容器中某一反应的A、B物质的量随时间变化的曲线如图所示,
某温度时.在2L密闭容器中某一反应的A、B物质的量随时间变化的曲线如图所示,