题目内容
14.利用下列装置(部分仪器已省略),能顺利完成对应实验的是( )| A. | 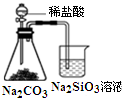 图所示实验可比较氯、碳、硅三种元素的非金属性强弱 | |
| B. | 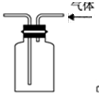 用图所示实验装置排空气法收集CO2气体 | |
| C. | 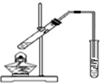 用图装置制备少量乙酸乙酯 | |
| D. | 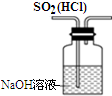 图装置可以用来除去SO2中的HCl |
分析 A.比较角度错误,应用高氯酸;
B.二氧化碳应用向上排空法收集;
C.为防止倒吸,导管不能插入液面以下;
D.二者都与氢氧化钠反应.
解答 解:A.比较非金属性,应用最高价氧化物的水化物,这里应用高氯酸,故A错误;
B.二氧化碳密度比空气大,应用向上排空法收集,则进气管较长,故B错误;
C.制备乙酸乙酯,因杂质乙酸、乙醇易溶于水,为防止倒吸,导管不能插入液面以下,故C正确;
D.二者都与氢氧化钠反应,应用饱和亚硫酸氢钠溶液吸收,故D错误.
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及酸性与非金属性的比较、气体的收集等,把握物质的性质、反应原理、实验技能为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
相关题目
5.将一定量的Na、Na2O、Na2O2的混合物与足量的水反应,在标准状况下得到a L混合气体.将该混合气体通过电火花引燃,恰好完全反应,则原混合物中Na、Na2O、Na2O2的物质的量之比可能为( )
| A. | 2:1:1 | B. | 1:1:2 | C. | 1:2:1 | D. | 4:3:3 |
19.下列反应属于氮的固定的是( )
| A. | NH4Cl与Ca(OH)2反应生成NH3 | B. | 空气在雷电作用下所产生NO | ||
| C. | NO和O2生成NO2 | D. | 铜与浓硝酸反应产生NO2 |
6.下列叙述正确的是( )
| A. | 固体时能导电的晶体一定为金属晶体 | |
| B. | 某晶体固态不导电,水溶液能导电,该晶体一定为离子晶体 | |
| C. | 某晶体难溶于水、熔点高、固态不导电,熔化时导电,可判断该晶体为离子晶体 | |
| D. | 由原子构成的晶体均具有熔沸点高、硬度大的特性 |
3.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA | |
| B. | 高温下,0.3molFe与足量水蒸气反应,生成的H2的体积为8.96L | |
| C. | 1mol Na2O2固体中含离子总数为4 NA | |
| D. | 标准状况下6.72 L NO2与水反应转移的电子数0.1NA |
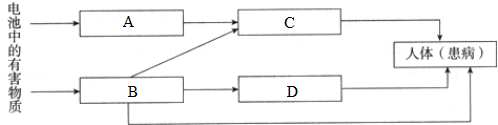
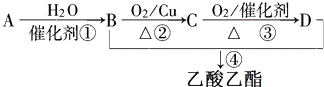
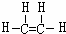 .
.