题目内容
9.某元素R的最高价氧化物对应的水化物是HnRO2n,则在气态氢化物中R元素的化合价是( )| A. | 3n | B. | 3n-8 | C. | -3n | D. | 8-3n |
分析 根据HnRO2n利用化合价代数和为0计算R元素的最高化合价,再利用最高正化合价-8=最低负价,即为气态氢化物中R元素的化合价,据此计算.
解答 解:令HnRO2n中R元素的化合价为x,
由化合物化合价代数和为0,所以(+1)×n+x+(-2)×2n=0,
解得x=3n,
所以最低负价为3n-8,
故选B.
点评 本题考查化合价的计算,题目难度不大,关键利用化合价代数和为0计算R元素的最高化合价,再利用最高正化合价-8=最低负价.

练习册系列答案
相关题目
4.下列有关原子核外电子排布的说法正确的是( )
| A. | 原子核外的电子总是尽先排在能量高的电子层里,然后才排在能量低的电子层 | |
| B. | 某原子的核电荷数与最外层电子数相等 | |
| C. | 原子核外的电子层分为七层,每层所排的电子数相同 | |
| D. | 某原子M层上电子数是L层上电子数的4倍 |
14.已知直链烷烃A比B多一个碳原子,则下列说法正确的是( )
| A. | A沸点比B高 | |
| B. | A相对密度比B小 | |
| C. | 一般情况下,同碳原子的烷烃的沸点和密度低于烯烃 | |
| D. | 已知A在常温下为液态,则B不可能为气态 |
1.将固体NH4I置于密闭容器中,在一定温度下发生下列反应:
①NH4I(s)?NH3(g)+HI(g);
②2HI(g)?H2(g)+I2(g)
达到平衡时,c(H2)=0.25mol/L,c(HI)=5mol/L,
则此温度下反应①的平衡常数(单位:mol2•L-2)为( )
①NH4I(s)?NH3(g)+HI(g);
②2HI(g)?H2(g)+I2(g)
达到平衡时,c(H2)=0.25mol/L,c(HI)=5mol/L,
则此温度下反应①的平衡常数(单位:mol2•L-2)为( )
| A. | 25 | B. | 0.025 | C. | 30.25 | D. | 27.5 |
18.将下列浓溶液蒸干并灼烧,可以得到原溶质的是( )
| A. | 氯化钠 | B. | 碳酸氢钠 | C. | 偏铝酸钠 | D. | 氯化铁 |

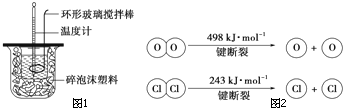 针对化学反应中的能量变化解决下列问题.
针对化学反应中的能量变化解决下列问题. 2,3,4,5-四甲基己烷
2,3,4,5-四甲基己烷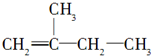 2-甲基-1丁烯
2-甲基-1丁烯 .
. .
. 分子式为C10H20,按碳的骨架分,该有机物属于ab.(填字母序号)
分子式为C10H20,按碳的骨架分,该有机物属于ab.(填字母序号)