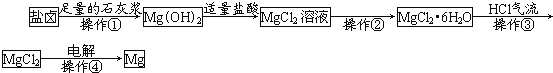题目内容
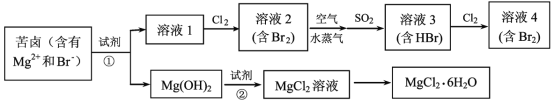
【题目】海水是巨大的资源宝库,工业上从海水中提取食盐和溴的过程如图:

操作Ⅱ发生反应的离子方程式为___;如果用碳酸钠溶液代替操作Ⅱ中的二氧化硫水溶液,则生成物中溴的化合价分别为+5和﹣1价,且操作Ⅲ中用稀硫酸代替氯气,请写出这种情况下操作Ⅲ中发生反应的离子方程式:___。
【答案】SO2+Br2+2H2O=SO42-+2Br-+4H+ BrO3-+5Br-+6H+=3Br2+3H2O
【解析】
海水淡化得到氯化钠,电解氯化钠溶液或熔融状态氯化钠会生成氯气,氯气通入母液中发生反应得到低浓度的溴单质溶液,通入热空气吹出后用二氧化硫水溶液吸收得到含HBr的溶液,通入适量氯气氧化得到溴单质,富集溴元素,蒸馏得到工业溴,
步骤Ⅱ用SO2水溶液吸收Br2,使溴蒸气转化为氢溴酸以达到富集的目的;生成物中溴的化合价分别为+5和-1价,在酸性条件下可发生归中反应生成溴,根据电子得失守恒配平;
操作Ⅱ是二氧化硫吸收溴单质发生反应生成硫酸和溴化氢,使溴蒸气转化为氢溴酸以达到富集的目的.其反应离子方程式为:SO2+Br2+2H2O═SO42﹣+2Br﹣+4H+,用碳酸钠溶液代替操作Ⅱ中的二氧化硫水溶液,生成物中溴的化合价分别为+5和﹣1价,操作Ⅲ中发生的反应是在酸性条件下归中反应生成溴,反应的方程式为:BrO3﹣+5Br﹣+6H+=3Br2+3H2O,故答案为:SO2+Br2+2H2O═SO42﹣+2Br﹣+4H+;BrO3﹣+5Br﹣+6H+=3Br2+3H2O;

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目