题目内容
【题目】下列图示与对应的叙述相符的是
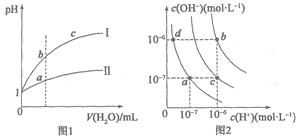
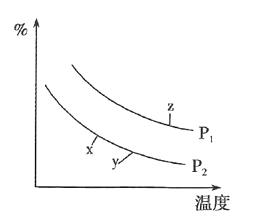
A.图1表示相同温度下pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线II为盐酸,且b点溶液的导电性比a点强
B.图1中,中和等体积的两种酸,消耗等浓度的NaOH溶液体积V(I)>V(II)
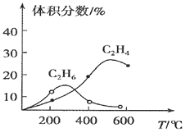
C.图2中纯水仅升高温度,就可以从a点变到c点
D.图2中在b点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显中性
【答案】D
【解析】
在图Ⅰ中,盐酸与醋酸的pH相同,加水稀释相同的倍数后,盐酸溶液的pH变化大,所以Ⅰ为盐酸,Ⅱ为醋酸。
A.相同pH的盐酸和醋酸分别加水稀释相同倍数时,盐酸的pH变化大,所以曲线Ⅰ应为盐酸,A错误;
B. 因为盐酸和醋酸的pH相同,所以醋酸溶液的浓度大,中和等体积的两种酸,消耗等浓度的NaOH溶液体积V(I)< V(II),B错误;
C. 图2中纯水仅升高温度,c(H+)、c(OH-)同等程度增大且相等,不可能从a点变到c点,C错误;
D. 图2中在b点对应温度下,KW=10-12,pH=2的H2SO4中,c(H+)=10-2mol/L;pH=10的NaOH溶液中,c(OH-)=10-2mol/L,二者等体积混合后,刚好完全反应,溶液呈中性,D正确。
故选D。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目