��Ŀ����
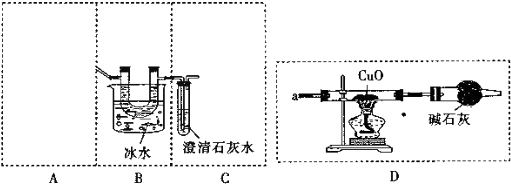
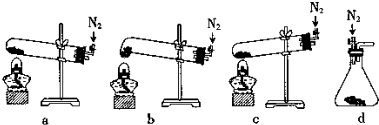
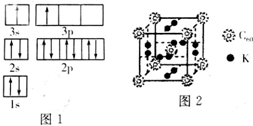
16���ߴ����������Ϣ�����Ĺؼ����ϣ���1����ҵ����ʯӢɰ�ͽ�̿���Ƶôֹ裮��֪��ͼ1��ͼ2�뽫���·�Ӧ���Ȼ�ѧ����ʽ����������SiO2��s��+2C��s���TSi��s��+2CO��g����H=+638.4 kJ•mol-1
��2���ֹ辭ϵ�з�Ӧ�����ɹ��飨SiH4��������ֽ����ɸߴ��裮��֪����ķֽ��¶�Զ���ڼ��飬��ԭ�ӽṹ������ԭ��C��Si������������ͬ��Cԭ�Ӱ뾶С��Si��
��3�����ֹ�ת����������裨SiHCl3������һ����ӦҲ���Ƶøߴ��裮
��SiHCl3�к��е�SiCl4��AsCl3�����ʶԾ�����������Ӱ�죮�����±����ݣ�
��������������ᴿSiHCl3��
| ���� | SiHCl3 | SiCl4 | AsCl3 |
| �е�/�� | 32.0 | 57.5 | 131.6 |
����˵����ȷ����ac������ĸ��ţ���
a���÷�Ӧ��ƽ�ⳣ�����¶����߶�����
b���������ʾ��Ͷ�ϱ�Ӧ����n��SiHCl3��/n�� H2��
c��ʵ��������Ϊ���SiHCl3�������ʣ�Ӧ�ʵ������¶�
���������������������������������ȼ�ṩ���ȼ�Ļ����豸�����ӽ���Ĥ���ۣ���ͼ4��ʾ�������н��������ҵ���Һ�Ǿ��Ƶı���ʳ��ˮ��b�缫�ϵĵ缫��Ӧʽ��2H++2e-�TH2����
��4�����������������������������ҵ����SiO2��Na2CO3��CaCO3��283kg�ڸ�������ȫ��Ӧʱ�ų�CO2��44kg���������IJ������û�ѧʽNa2SiO3•CaSiO3•xSiO2��ʾ��������x=4��
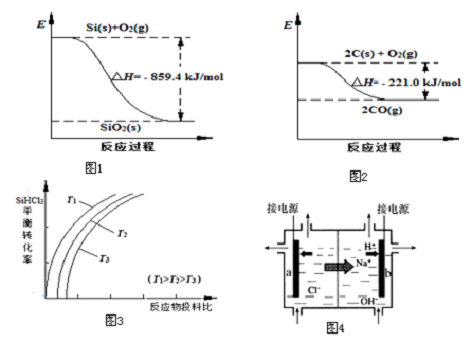
���� ��1������������Ӧ���������仯ͼ���֪��Si��s��+O2��s���TSiO2��s����H=-859.4 kJ•mol-1��2C��s��+O2��s���T2CO��g����H=-221.0 kJ•mol-1���õڶ�������ʽ��ȥ��һ������ʽ�ó����跴Ӧ��
��2��C��Si������������ͬ��Cԭ�Ӱ뾶С��Si����ѧ����ǿ�������ж��ȶ��ԣ�
��3���ٸ��ݸ����ʷе�IJ�ͬ�����ᴿ���ʣ��������������
��a����Ϊ�����¶ȵ����ߣ�SiHCl3��ת��������ƽ�����ƣ���÷�Ӧ��ƽ�ⳣ�����¶����߶�����
b������һ�ַ�Ӧ���Ũ�ȣ������������Ӧ���ת���ʣ���������ת���ʷ������ͣ��ʺ������ʾ��Ͷ�ϱ�Ӧ����$\frac{n��{H}_{2}��}{n��SiHC{l}_{3}��}$��
c����Ϊ�����¶ȵ����ߣ�SiHCl3��ת��������ƽ�����ƣ���ʵ��������Ϊ���SiHCl3�������ʣ�Ӧ�ʵ������¶ȣ�
���������������ӷŵ磬��������ʽӦ�����Ȼ��ƣ�b�缫���������������ڸü��ŵ磬���Ե缫��Ӧʽ��2H++2e-=H2����
��4���ɷ���ʽNa2CO3+SiO2$\frac{\underline{\;����\;}}{\;}$NaSiO3+CO2����CaCO3+SiO2$\frac{\underline{\;����\;}}{\;}$CaSiO3+CO2�������Է�Ӧ������n��CO2��=n��Na2CO3��+n��CaCO3��=n��SiO2��Ӧ����
��� �⣺��1������������Ӧ���������仯ͼ���֪��Si��s��+O2��s���TSiO2��s����H=-859.4 kJ•mol-1
2C��s��+O2��s���T2CO��g����H=-221.0 kJ•mol-1���õڶ�������ʽ��ȥ��һ������ʽ�ó����跴Ӧ��SiO2��s��+2C��s���TSi��s��+2CO��g����H=+638.4 kJ•mol-1���õ���H=+638.4 kJ•mol-1��
�ʴ�Ϊ��+638.4 kJ•mol-1��
��2������ķֽ��¶�Զ���ڼ��飬����ΪC��Si������������ͬ��Cԭ�Ӱ뾶С��Si��SiԪ�صķǽ���������CԪ�أ���������ȶ������ڼ��飬
�ʴ�Ϊ��C��Si������������ͬ��Cԭ�Ӱ뾶С��Si��
��3���ٸ��ݸ����ʷе�IJ�ͬ�����ᴿ���ʣ���������������ʴ�Ϊ���������
��a����Ϊ�����¶ȵ����ߣ�SiHCl3��ת��������ƽ�����ƣ���÷�Ӧ��ƽ�ⳣ�����¶����߶�����a��ȷ��
b������һ�ַ�Ӧ���Ũ�ȣ������������Ӧ���ת���ʣ���������ת���ʷ������ͣ��ʺ������ʾ��Ͷ�ϱ�Ӧ����$\frac{n��{H}_{2}��}{n��SiHC{l}_{3}��}$����b����
c����Ϊ�����¶ȵ����ߣ�SiHCl3��ת��������ƽ�����ƣ���ʵ��������Ϊ���SiHCl3�������ʣ�Ӧ�ʵ������¶ȣ���c��ȷ��
��ѡac��
���������������ӷŵ磬��������ʽӦ�����Ȼ��ƣ�b�缫���������������ڸü��ŵ磬���Ե缫��Ӧʽ��2H++2e-=H2����
�ʴ�Ϊ�����Ƶı���ʳ��ˮ��2H++2e-�TH2��
��4�������Ļ�ѧ��ɿɸ��ݷ�Ӧԭ���õ���
Na2CO3+SiO2$\frac{\underline{\;����\;}}{\;}$NaSiO3+CO2����CaCO3+SiO2$\frac{\underline{\;����\;}}{\;}$CaSiO3+CO2����
�ɻ�ѧʽNa2SiO3•CaSiO3•xSiO2��Ӧ��Na2CO3��CaCO3�����ʵ�����ȣ�
n��CO2��=n��Na2CO3��+n��CaCO3��=n��SiO2��Ӧ��=$\frac{44kg}{44g}$=1000mol��
n��Na2CO3��=n��CaCO3��=500mol
500molNa2CO3��������53kg��500molCaCO3��������50kg��1000molSiO2��������60kg��
n��SiO2������=$\frac{283kg-50kg-53kg-60kg}{60g}$=2000mol��
��ʣ��Ķ�����������ɵĹ���ơ�������Ϊ2000��500��500=4��1��1��
����x=4���ʴ�Ϊ��4��
���� ������Ҫ�������Ԫ�����ڱ���Ӧ�á���˹����Ӧ�á���ѧƽ�ⳣ����ƽ���ƶ��ȣ���Ŀ�Ѷ��еȣ�ע�����֪ʶ�Ļ��ۣ�

 ÿ�α���ϵ�д�
ÿ�α���ϵ�д� ��ѧ����ϵ�д�
��ѧ����ϵ�д�| A�� | 10mL 0.5mol/L CH3COONa��Һ��6mL 1mol/L�����ϣ�c��Cl-����c��Na+����c��CH3COO-����c��H+����c��OH-�� | |
| B�� | ��Ũ�ȵ�����ϡ��Һ������������ �������� �۴��� ��̼������ �������� �ޱ����ƣ����ǵ�pH��С��������Ϊ���ۢݢ٢ܢڢ� | |
| C�� | ������0.1 mol/L��������Һ ��NH4Al��SO4��2 ��NH4Cl ��NH3•H2O ��CH3COONH4��c ��NH4+���ɴ�С��˳���ǣ��ڣ��٣��ܣ��� | |
| D�� | ��25��ʱ����a mol•L-1�İ�ˮ��0.01 mol•L-1������������Ϸ�Ӧʱ��Һ��c��NH4+��=c��Cl-�����ú�a�Ĵ���ʽ��ʾNH3•H2O�ĵ��볣��Kb=$\frac{1{0}^{-9}}{a-0.01}$ |
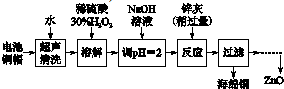
��1����ͭñ�ܽ�ʱ����H2O2��Ŀ����Cu+H2O2+H2SO4=CuSO4+2H2O ���û�ѧ����ʽ��ʾ����
��ͭñ�ܽ���ȫ���轫��Һ�й�����H2O2��ȥ����ȥH2O2�ļ�㷽���Ǽ������У�
��2��Ϊȷ������п�ң���Ҫ�ɷ�ΪZn��ZnO������Ϊ�����������������ʵ������ⶨ��ȥH2O2����Һ��Cu2+�ĺ�����ʵ�����Ϊ��ȷ��ȡһ������ĺ���Cu2+����Һ�ڴ�����ƿ�У�������ˮϡ�ͣ�������ҺpH=3��4�����������KI����Na2S2O3����Һ�ζ����յ㣮���������з�Ӧ�����ӷ���ʽ���£�
2Cu2++4I-�T2CuI����ɫ����+I2 2S2O+I2�T2I-+S4O62-
�ٵζ�ѡ�õ�ָʾ��Ϊ������Һ���ζ��յ�۲쵽��������ɫ��ȥ��30�벻�ָ���ɫ��
�����ζ�ǰ��Һ�е�H2O2û�г��������ⶨ��Cu2+��������ƫ�ߣ��ƫ�ߡ�����ƫ�͡����䡱����
��3����֪pH��11ʱZn��OH��2������NaOH��Һ����[Zn��OH��4]2-���±��г��˼������������������������pH����ʼ������pH����������Ũ��Ϊ1.0mol•L-1���㣩��
| ��ʼ������pH | ������ȫ��pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 9 |
�ɳ�ȥͭ����Һ�Ʊ�ZnO����ȷʵ�鲽������Ϊ���ݢܢ٢ڢۢ�
�ٹ��ˣ�
�ڵ�����ҺpHԼΪ10����8.9��pH��11����ʹZn2+������ȫ��
�۹��ˡ�ϴ�ӡ����
�ܵ�����ҺpHԼΪ5����3.2��pH��5.9����ʹFe3+������ȫ��
������Һ�м�������30% H2O2��ʹ���ַ�Ӧ��
��900�����գ�
��4��Zn��OH��2���ܶȻ�����Ϊ1.2��10-17��mol•L-1��3����Zn2+������ȫʱ����ʱ��Һ��Zn2+��Ũ��Ϊ1.2��10-7 mol•L-1��
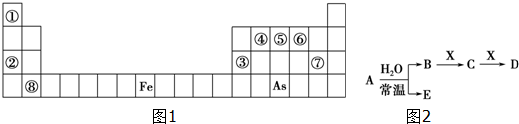
 �������ƳɵĽ���ȼ�ϡ��ǽ�������ȼ�ϵ���Ӧ�õ��������߿Ƽ�����λ������A��B����ȼ��ʱ���ų������ȣ�������ȼ�ϣ���֪A��B��Ϊ������Ԫ�أ���ԭ�ӵĵ�һ�����ĵ��������±���ʾ��
�������ƳɵĽ���ȼ�ϡ��ǽ�������ȼ�ϵ���Ӧ�õ��������߿Ƽ�����λ������A��B����ȼ��ʱ���ų������ȣ�������ȼ�ϣ���֪A��B��Ϊ������Ԫ�أ���ԭ�ӵĵ�һ�����ĵ��������±���ʾ��| �������ܣ�KJ•mol�� | ��I1 | ��I2 | ��I3 | ��I4 |
| ��A | ��932 | ��1821 | ��15390 | ��21771 |
| ��B | ��738 | ��1541 | ��7733 | ��10540 |
��2��ACl2������A���ӻ�����Ϊsp�ӻ���
��3����ѧ�Ұ�C60�ͼز�����һ��������һ�ָ���ϩ������侧����ͼ2��ʾ���������ڵ���ʱ��һ�ֳ����壮��̬��ԭ�ӵļ۵����Ų�ʽΪ4S1����������Kԭ�Ӻ�C60���ӵĸ�����Ϊ3��1��
��4����C60��ѧ���ֺϳ���Si60��N60��C��Si��Nԭ�ӵ縺���ɴ�С��˳����N��C��Si��NCl3���ӵļ۲���ӶԻ�������ģ��Ϊ�������壮Si60������ÿ����ԭ��ֻ�����ڵ�3����ԭ���γɹ��ۼ�����ÿ����ԭ������㶼����8�����ȶ��ṹ��������Цм�����ĿΪ30��