题目内容
下列实验正确的是
| A.用量筒量取15.50mL 0.100 mol·L-1盐酸 |
| B.用无水酒精萃取碘水中的碘 |
| C.用过量浓氨水洗涤试管内的银镜 |
| D.做H2还原CuO实验时,要先通氢气,验纯后再加热 |
D
解析试题分析:量筒的精确度大约为0.1mL,酸式滴定管的精确度大约为0.01mL,因此量筒不能达到实验目的,应选酸式滴定管,故A选项错误;酒精就是乙醇,乙醇与水以任意比例互溶,不能作碘水的萃取剂,应选择不溶于水的四氯化碳、苯等有机溶剂,故B选项错误;银镜的主要成分是单质银,不是银离子,不能容于氨水,易溶于稀硝酸或浓硝酸,应选硝酸溶解,故C选项错误;为了防止被氢气还原出的单质铜被空气中的氧气氧化,要先通氢气,验纯后再加热,故D选项正确。
考点:考查化学实验基本操作,涉及量筒的使用、碘水的萃取剂、乙醇的溶解性、浓氨水的性质、洗涤银镜的试剂、氢气还原氧化铜的注意事项等。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
“封管试验”具有简易、方便、节约、绿色等优点。观察下列四个“封管试验”(夹持装置未画出),判断下列说法正确的是
| A.加热时,a上部聚集了固体NH4Cl,说明NH4C1的热稳性比较好 |
| B.加热时,发现b中I2变为紫色蒸气,在上部又聚集为紫黑色的固体 |
| C.加热时,c中溶液红色变深,冷却后又变浅 |
| D.水浴时,d内气体颜色变浅,e内气体颜色加深 |
下列实验操作正确且能达到目的是
| A.将AlCl3溶液蒸发结晶提取无水AlCl3 |
| B.在温水瓶中加入Na2CO3溶液泡浸后加入盐酸能除去内壁CaSO4 |
| C.用饱和的NaOH热溶液除去乙酸乙酯中的乙醇、乙酸 |
| D.将Cl2、HCl混合气体通过盛有NaHCO3饱和溶液的洗气瓶除去HCl |
关于下列图示的说法中,正确的是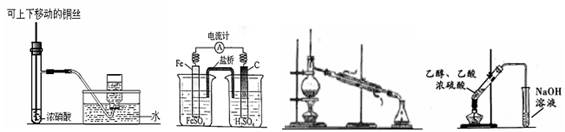
图1 图2 图3 图4
| A.图1制备并收集少量NO2气体 |
| B.图2是原电池装置,Fe电极为负极 |
| C.图3常用于分离互不相溶的液体 |
| D.图4可用于实验室制取和收集乙酸乙酯 |
下列叙述错误的是
| A.易燃试剂应与强氧化性试剂分开放置并远离火源 |
| B.某溶液中加入盐酸,有白色沉淀生成,说明原溶液中一定存在Ag+ |
| C.用50 mL酸式滴定管可准确量取25.00 mL的KMnO4溶液 |
| D.氢氧化铁胶体加热蒸干、灼烧后有氧化铁生成 |
下列说法不正确的是
| A.燃着的酒精灯不慎碰翻失火,应该迅速用湿抹布扑盖 |
| B.用电子天平称量化学药品时,必须先称小烧杯的质量,再称量加入试剂后的总质量,两者之差即为药品的质量。 |
| C.制备摩尔盐的过程中,洗涤硫酸亚铁铵晶体时,应用少量酒精洗去晶体表面附着的水分 |
| D.在适量氯化钴的乙醇溶液中,逐滴加入水至溶液恰好呈粉红色,加热该溶液,结果依次呈现紫色、蓝紫色、蓝色的变化 |
下列装置不能完成实验的是 ( )
| | 装置 | 实验 | | 装置 | 实验 |
| A |  | 结合秒表测 量锌与硫酸 的反应速率 | C | 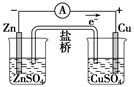 | 验证化学能 转化为电能 |
| B | 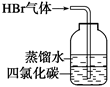 | 吸收多余 HBr气体 | D | 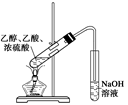 | 实验室制 取少量乙酸 乙酯 |
工业上以锂辉石(Li2O·Al2O3·4SiO2,含少量Ca、Mg元素)为原料生产碳酸锂。其部分工艺流程如下: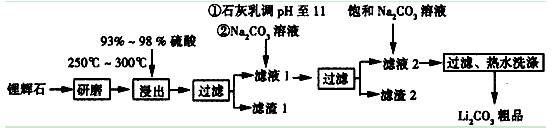
已知:①Li2O·Al2O3·4SiO2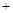 H2SO4(浓)
H2SO4(浓) Li2SO4
Li2SO4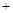 Al2O3·4SiO2·H2O↓
Al2O3·4SiO2·H2O↓
②某些物质的溶解度(S)如下表所示:
| T/℃ | 20 | 40 | 60 | 80 |
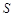 (Li2CO3)/g (Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
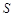 (Li2SO4)/g (Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
③从滤渣1中提取出Si的部分流程如下图所示:

根据以上信息,请回答下列问题:
(1)括号内应提供的相应条件和物质 、 。
(2)方框中所得物质的化学式 。
(3)使用浓硫酸并加热到250℃~300℃的目的是 。
(4)②处加Na2CO3溶液所发生反应的离子方程式 、 。
(5)滤渣2的主要成分有 。
(6)如何检验Li2CO3是否洗涤干净? 。
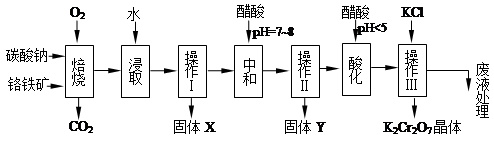
 8Na2CrO4+2 Fe2O3+8CO2↑;
8Na2CrO4+2 Fe2O3+8CO2↑; 2CrO42-+2H+
2CrO42-+2H+