题目内容
关于下列图示的说法中,正确的是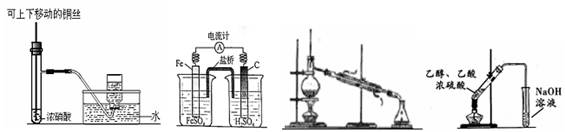
图1 图2 图3 图4
| A.图1制备并收集少量NO2气体 |
| B.图2是原电池装置,Fe电极为负极 |
| C.图3常用于分离互不相溶的液体 |
| D.图4可用于实验室制取和收集乙酸乙酯 |
B
解析试题分析:铜与浓硝酸反应可以制备NO2,但是NO2易溶于水,与水反应生成硝酸和NO,因此不能用排水法收集NO2,只能用向上排空气法收集,故A选项错误;铁与稀硫酸能发生置换反应,Fe比C容易失去电子,则图2是原电池,Fe是负极,C是正极,故B选项正确;图3代表蒸馏,用于分离互溶液体混合物,且各组成成分的沸点相差较大,分离互不相溶的液体的操作是分液,故C选项错误;乙醇、乙酸在浓硫酸催化加热下发生酯化反应,可以制备乙酸乙酯,但是不能用NaOH溶液除去乙酸乙酯中混入的少量乙醇和乙酸,因为乙酸乙酯也能与NaOH溶液反应,应选择饱和Na2CO3溶液除杂,故D选项错误。
考点:考查化学实验基本操作,主要涉及二氧化氮的实验室制法、原电池的 构成条件和电极类型、混合物分离提纯的常见方法、乙酸乙酯的制法和提纯等。

练习册系列答案
相关题目
下列试管实验的方案中,一定能达到实验目的是
| A.制备乙酸丁酯:加入正丁醇和乙酸,再滴加几滴浓硫酸,振荡,水浴加热 |
B.检验甲基橙试液中是否混有微量酚酞:按图所示上升纸上层析法实验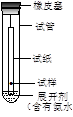 |
| C.检验醛基:加入CuSO4溶液和NaOH溶液各1mL,振荡,加入乙醛溶液,煮沸 |
| D.比较苯酚、乙酸、碳酸的酸性:乙酸和纯碱反应产生的气体通入苯酚钠溶液中 |
下列根据实验操作和现象所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结 论 |
| A | 向溶液X中先滴加稀硝酸,再滴加Ba(NO3)2溶液 | 出现白色沉淀 | 溶液X中一定含有SO42- |
| B | 等体积pH=3的HA和HB两种酸分别与足量的锌反应,排水法收集气体 | HA放出的氢气多且反应速率快 | HB酸性比HA强 |
| C | 溴乙烷与NaOH溶液共热后,滴加AgNO3溶液 | 未出现淡黄色沉淀 | 溴乙烷未发生水解 |
| D | 向1mL1%的NaOH溶液中加入2mL2%的CuSO4溶液,振荡后再加入0.5mL有机物Y,加热 | 未出现砖红色沉淀 | Y中不含有醛基 |
下列有关实验操作正确的是
| A.用固体氯化铵和氢氧化钙制取氨气结束后,将大试管从铁架台上取下立即进行洗涤 |
| B.用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 |
| C.做金属钠的性质实验时,剩余的钠放回原试剂瓶 |
| D.向沸腾的NaOH稀溶液中滴入FeCl3饱和溶液,来制备Fe(OH)3胶体 |
下列实验正确的是
| A.用量筒量取15.50mL 0.100 mol·L-1盐酸 |
| B.用无水酒精萃取碘水中的碘 |
| C.用过量浓氨水洗涤试管内的银镜 |
| D.做H2还原CuO实验时,要先通氢气,验纯后再加热 |
下列关于实验的说法正确的是
| A.用玻璃棒蘸取NaOH溶液,滴在pH试纸上,马上和比色卡对照,确定NaOH的pH |
| B.滴定用的滴定管、锥形瓶和配制一定物质的量浓度溶液用的容量瓶,使用前均要润洗 |
| C.均不能采取将溶液直接蒸干的方法制得AlCl3、Al2(SO4)3、FeCl3、Fe2(SO4)3 |
| D.因为Ksp(CaCO3)<Ksp(CaSO4),所以可用Na2CO3和HCl除去水垢中的CaSO4 |
下列与实验相关的叙述中,正确的是 ( )
| A.将碘水倒入分液漏斗,再加适量苯,充分振荡、静置、过滤,可从碘水中获取碘 |
| B.从CuSO4溶液得到CuSO4·5H2O的操作是加热浓缩,冷却结晶 、过滤、洗涤、干燥 |
| C.室温下向滴有酚酞的NaOH溶液中滴加稀盐酸当红色恰好退去时所得溶液pH=7 |
| D.向某溶液中滴加氯水后,滴加KSCN溶液,溶液变红,证明溶液中含有Fe2+ |