题目内容
已知25℃,醋酸、次氯酸、碳酸、亚硫酸的电离平衡常数如表,下列叙述正确的是( )
| 酸 | 电离平衡常数 |
| 醋酸 | Ki=1.75×10-5 |
| 次氯酸 | Ki=2.98×10-8 |
| 碳酸 | Ki1=4.30×10-7 Ki2=5.61×10-11 |
| 亚硫酸 | Ki1=1.54×10-2 Ki2=1.02×10-7 |
| A、25℃,等pH值的CH3COONa、NaClO、Na2CO3和Na2SO3四种溶液中,物质的量最小的是Na2CO3 |
| B、少量的SO2通入NaClO溶液中反应的离子方程式为:SO2+H2O+2ClO-→SO32-+2HClO |
| C、少量CO2通入Ca(ClO)2溶液中反应的离子方程式为:CO2+H2O+ClO-→HCO3-+HClO |
| D、向pH=a的醋酸溶液中加一定量水,所得溶液的pH>a、pH<a、pH=a均有可能 |
考点:弱电解质在水溶液中的电离平衡,电解质与非电解质
专题:电离平衡与溶液的pH专题
分析:根据表中电离平衡常数可知,酸性大小:醋酸>亚硫酸>碳酸>亚硫酸氢根离子>次氯酸>碳酸氢根离子,
A.弱酸的钠盐溶液中,酸越弱,其水解程度越大,则钠盐溶液的碱性越强,据此进行判断;
B.由于反应生成的次氯酸具有强氧化性,能够将亚硫酸根离子氧化成硫酸根离子;
C.次氯酸的酸性大于碳酸氢根离子,所以反应生成次氯酸和碳酸氢根离子;
D.醋酸为酸,加入水稀释的过程中氢离子浓度减小,溶液的pH一定大于a.
A.弱酸的钠盐溶液中,酸越弱,其水解程度越大,则钠盐溶液的碱性越强,据此进行判断;
B.由于反应生成的次氯酸具有强氧化性,能够将亚硫酸根离子氧化成硫酸根离子;
C.次氯酸的酸性大于碳酸氢根离子,所以反应生成次氯酸和碳酸氢根离子;
D.醋酸为酸,加入水稀释的过程中氢离子浓度减小,溶液的pH一定大于a.
解答:
解:根据表中数据可知,酸性大小关系为:醋酸>亚硫酸>碳酸>亚硫酸氢根离子>次氯酸>碳酸氢根离子,
A.相同物质的量浓度的含有弱酸根离子的钠盐溶液,对应酸的酸性越弱则酸根离子水解程度越大,溶液中氢氧根离子浓度越大,pH越大,水解程度大小顺序是:CH3COO-<SO32-<ClO-<CO32-,所以相同温度时,等pH的CH3COONa、NaClO、Na2CO3和Na2SO3四种溶液中,物质的量浓度最小的为水解程度最大的盐:碳酸钠,由于没有告诉溶液体积,各物质的物质的量大小无法判断,故A错误;
B.少量的SO2通入NaClO溶液中,反应生成的次氯酸能够氧化亚硫酸根离子,正确的离子方程式为:SO2+H2O+ClO-→SO42-+2H++Cl-,故B错误;
C.CO2通入Ca(ClO)2溶液中,反应生成次氯酸和碳酸氢根离子,反应的离子方程式为:CO2+H2O+ClO-→HCO3-+HClO,故C正确;
D.向pH=a的醋酸溶液中加一定量水,醋酸的电离程度增大,但是溶液中氢离子浓度减小,溶液的pH增大,即pH>a,故D错误;
故选C.
A.相同物质的量浓度的含有弱酸根离子的钠盐溶液,对应酸的酸性越弱则酸根离子水解程度越大,溶液中氢氧根离子浓度越大,pH越大,水解程度大小顺序是:CH3COO-<SO32-<ClO-<CO32-,所以相同温度时,等pH的CH3COONa、NaClO、Na2CO3和Na2SO3四种溶液中,物质的量浓度最小的为水解程度最大的盐:碳酸钠,由于没有告诉溶液体积,各物质的物质的量大小无法判断,故A错误;
B.少量的SO2通入NaClO溶液中,反应生成的次氯酸能够氧化亚硫酸根离子,正确的离子方程式为:SO2+H2O+ClO-→SO42-+2H++Cl-,故B错误;
C.CO2通入Ca(ClO)2溶液中,反应生成次氯酸和碳酸氢根离子,反应的离子方程式为:CO2+H2O+ClO-→HCO3-+HClO,故C正确;
D.向pH=a的醋酸溶液中加一定量水,醋酸的电离程度增大,但是溶液中氢离子浓度减小,溶液的pH增大,即pH>a,故D错误;
故选C.
点评:本题考查了弱电解质的电离平衡、离子方程式的书写,题目难度中等,注意掌握弱电解质的电离平衡及其影响因素,能够正确书写离子方程式,选项B为易错点,注意次氯酸的强氧化性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
钡离子具有毒性,但在肠胃放射性检查中,却常服用“钡餐”.为减少微量溶解的钡离子对人体的伤害,“钡餐”中含有一种保护成分,其可能为( )
| A、碳酸钡 | B、硫酸钠 |
| C、稀硫酸 | D、碳酸钠 |
我国稀土资源丰富.下列有关稀土元素
Ce、
Ce的说法正确的是( )
136 58 |
138 58 |
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
下列有关物质的用途(括号内为用途)错误的是( )
| A、硅(半导体材料) |
| B、二氧化硅(制光导纤维材料) |
| C、水玻璃(黏合剂) |
| D、硅酸(作耐火材料) |
下列表示溶液中所发生反应的离子方程式正确的是( )
| A、AlCl3溶液与过量氨水混合:Al3++4NH3?H2O═AlO2-+4NH4++2H2O | ||||
| B、偏铝酸钠溶液中通入过量二氧化碳:2AlO2-+CO2+2H2O═2Al(OH)3↓+CO32- | ||||
C、用铜电极做盐酸的导电实验:2H++2Cl-
| ||||
| D、向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀:2Ba2++NH4++Al3++2SO42-+4OH-═Al(OH)3↓+NH3?H2O+2BaSO4↓ |
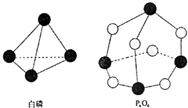 化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能量.已知白磷和P4O6的分子结构如右图所示,现提供以下化学键的键能(kJ?mol-1)P-P:198 P-O:360 O═O:498则反应P4(白磷)+3O2→P4O6的能量变化为( )
化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能量.已知白磷和P4O6的分子结构如右图所示,现提供以下化学键的键能(kJ?mol-1)P-P:198 P-O:360 O═O:498则反应P4(白磷)+3O2→P4O6的能量变化为( )| A、释放1638kJ的能量 |
| B、吸收1638kJ的能量 |
| C、释放126kJ的能量 |
| D、吸收126kJ的能量 |
实验室用于检验盐酸和其他电离时能产生Cl-的化合物的试剂是( )
| A、稀盐酸和石灰水 |
| B、氢氧化铁 |
| C、氯化钡溶液和稀硝酸 |
| D、硝酸银溶液和稀硝酸 |
设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A、标准状况下,0.1mol Cl2溶于水,转移的电子数目为0.1NA |
| B、常温常压下,64g S02含有的原子总数为3NA |
| C、标准状况下,11.2L SO3中含有分子的数目为0.5NA |
| D、常温常压下,1mol Na2O2中阴离子数为2NA |