题目内容
我国稀土资源丰富.下列有关稀土元素
Ce、
Ce的说法正确的是( )
136 58 |
138 58 |
A、
| ||||
B、
| ||||
C、
| ||||
D、
|
考点:核素,质量数与质子数、中子数之间的相互关系
专题:原子组成与结构专题
分析:A.有相同质子数,不同中子数的原子互为同位素;
B.
Ce的质量数为136,
Ce的质量数为138;
C.核素是指具有一定数目质子和一定数目中子的同一种原子;
D.
Ce的电子数=质子数=58,中子数=质量数-质子数=136-58=78;
Ce的电子数=质子数=58,中子数=质量数-质子数=138-58=80.
B.
136 58 |
138 58 |
C.核素是指具有一定数目质子和一定数目中子的同一种原子;
D.
136 58 |
138 58 |
解答:
解:A.
Ce和
Ce质子数相同,中子数相同,故互为同位素,故A正确;
B.
Ce的质量数为136,
Ce的质量数为138,故B错误;
C.
Ce和
Ce质子数不同,为两种不同的核素,故C错误;
D.
Ce的电子数=质子数=58,中子数=质量数-质子数=136-58=78;
Ce的电子数=质子数=58,中子数=质量数-质子数=138-58=80,故D错误,
故选A.
136 58 |
138 58 |
B.
136 58 |
138 58 |
C.
136 58 |
138 58 |
D.
136 58 |
138 58 |
故选A.
点评:本题考查同位素、核素的概念,难度不大.对于元素、核素、同位素、同素异形体、同分异构体、同系物、同种物质等概念的区别是考试的热点问题.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
下列有机物不能通过乙烯的加成反应制取的是( )
| A、CH3CH2Cl |
| B、CH3-CHCl2 |
| C、CH3-CH2OH |
| D、CH3-COOH |
下列不属于有机物的是( )
| A、C6H6 |
| B、尿素 |
| C、醋酸 |
| D、碳铵 |
绿色电源“二甲醚-氧气燃料电池”的工作原理如图,所示下列说法正确的是( )
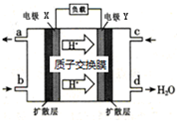

| A、氧气应从c处通入,电极Y上发生的反应为O2+4e-+2H2O═4OH- |
| B、电池在放电过程中,电极X周围溶液的pH增大 |
| C、二甲醚应从b处加入,电极X上发生的反应为(CH3)2O-12e-+3H2O=2CO2+12H+ |
| D、当该电池向外电路提供2mol电子时消耗O2约为22.4L |
设NA代表阿伏伽德罗常数的值,下列说法中正确的是( )
| A、NA个氯气分子与NA氢气分子的质量比等于35.5:1 |
| B、在常温常压下,11.2L氯气含有分子数为0.5NA |
| C、与7.8g Na2O2完全反应时,消耗H2O的分子数为0.2NA |
| D、1L 0.5mol?L-1硝酸钡溶液中所含NO3-数为0.5NA |
碲的某化合物就是常用的VCD光盘记录材料之一,碲位于钾的下一周期,与氧元素同一主族,对碲及其化合物的以下认识中不正确的是( )
| A、单质碲在常温下是固体 |
| B、H2TeO4的酸性比H2SO4的酸性弱 |
| C、H2Te不如HI稳定 |
| D、Te元素位于第六周期ⅥA族 |
下列反应属于氧化还原反应,且生成物的总能量大于反应物的总能量的是( )
| A、锌粒与稀硫酸的反应 |
| B、Ba(OH)2溶液与盐酸反应 |
| C、甲烷在氧气中的燃烧反应 |
| D、灼热的木炭与CO2反应 |
已知25℃,醋酸、次氯酸、碳酸、亚硫酸的电离平衡常数如表,下列叙述正确的是( )
| 酸 | 电离平衡常数 |
| 醋酸 | Ki=1.75×10-5 |
| 次氯酸 | Ki=2.98×10-8 |
| 碳酸 | Ki1=4.30×10-7 Ki2=5.61×10-11 |
| 亚硫酸 | Ki1=1.54×10-2 Ki2=1.02×10-7 |
| A、25℃,等pH值的CH3COONa、NaClO、Na2CO3和Na2SO3四种溶液中,物质的量最小的是Na2CO3 |
| B、少量的SO2通入NaClO溶液中反应的离子方程式为:SO2+H2O+2ClO-→SO32-+2HClO |
| C、少量CO2通入Ca(ClO)2溶液中反应的离子方程式为:CO2+H2O+ClO-→HCO3-+HClO |
| D、向pH=a的醋酸溶液中加一定量水,所得溶液的pH>a、pH<a、pH=a均有可能 |
第二周期元素,能与氧形成X2O5.则有关X的叙述正确的是( )
| A、X的单质在常温下以分子晶体形式存在 |
| B、X2O5的水化物是一种强酸 |
| C、X的氢化物在固态属于离子晶体 |
| D、X所在族元素的单质在固态时都属于同一晶体类型 |