题目内容
下列有关物质的用途(括号内为用途)错误的是( )
| A、硅(半导体材料) |
| B、二氧化硅(制光导纤维材料) |
| C、水玻璃(黏合剂) |
| D、硅酸(作耐火材料) |
考点:硅和二氧化硅
专题:碳族元素
分析:A.硅是制造半导体的主要材料;
B.二氧化硅是制造光导纤维的主要材料;
C.水玻璃具有粘性;
D.硅酸钠能作耐火材料,硅酸不能作耐火材料.
B.二氧化硅是制造光导纤维的主要材料;
C.水玻璃具有粘性;
D.硅酸钠能作耐火材料,硅酸不能作耐火材料.
解答:
解:A.硅元素处于金属和非金属元素分界线处,具有金属和非金属的性质,所以可以作半导体材料,故A正确;
B.二氧化硅是制造光导纤维的主要材料,是利用光的全反射原理,故B正确;
C.硅酸钠的水溶液俗称水玻璃,具有粘性,能作黏合剂,故C正确;
D.硅酸钠的水溶液俗称水玻璃,既不燃烧也不支持燃烧,可作耐火材料,硅酸在加热时分解生成二氧化硅和水,所以不能作耐火材料,故D错误;
故选D.
B.二氧化硅是制造光导纤维的主要材料,是利用光的全反射原理,故B正确;
C.硅酸钠的水溶液俗称水玻璃,具有粘性,能作黏合剂,故C正确;
D.硅酸钠的水溶液俗称水玻璃,既不燃烧也不支持燃烧,可作耐火材料,硅酸在加热时分解生成二氧化硅和水,所以不能作耐火材料,故D错误;
故选D.
点评:本题考查了硅及其化合物的用途,明确物质的性质是解本题关键,性质决定用途,注意基础知识的积累,题目难度不大.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
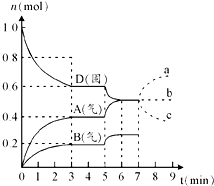 在容积为2.0L的密闭容器内,物质D在T℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,下列叙述不正确的是( )
在容积为2.0L的密闭容器内,物质D在T℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,下列叙述不正确的是( )| A、从反应开始到第一次达到平衡时,A物质的平均反应速率为0.667mol/(L?min) |
| B、该反应的化学方程式为2D(s)?2A(g)+B(g)该反应的平衡常数表达式为K=c(A)2?c(B) |
| C、已知反应的△H>0,则第5分钟时图象呈现上述变化的原因可能是升高体系的温度 |
| D、若在第7分钟时增加D的物质的量,则表示A的物质的量变化正确的是a曲线 |
绿色电源“二甲醚-氧气燃料电池”的工作原理如图,所示下列说法正确的是( )
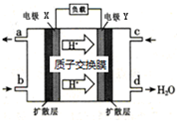

| A、氧气应从c处通入,电极Y上发生的反应为O2+4e-+2H2O═4OH- |
| B、电池在放电过程中,电极X周围溶液的pH增大 |
| C、二甲醚应从b处加入,电极X上发生的反应为(CH3)2O-12e-+3H2O=2CO2+12H+ |
| D、当该电池向外电路提供2mol电子时消耗O2约为22.4L |
碲的某化合物就是常用的VCD光盘记录材料之一,碲位于钾的下一周期,与氧元素同一主族,对碲及其化合物的以下认识中不正确的是( )
| A、单质碲在常温下是固体 |
| B、H2TeO4的酸性比H2SO4的酸性弱 |
| C、H2Te不如HI稳定 |
| D、Te元素位于第六周期ⅥA族 |
下列反应属于氧化还原反应,且生成物的总能量大于反应物的总能量的是( )
| A、锌粒与稀硫酸的反应 |
| B、Ba(OH)2溶液与盐酸反应 |
| C、甲烷在氧气中的燃烧反应 |
| D、灼热的木炭与CO2反应 |
已知某有机物A的红外光谱和核磁共振氢谱如图所示,下列说法不正确的是( )
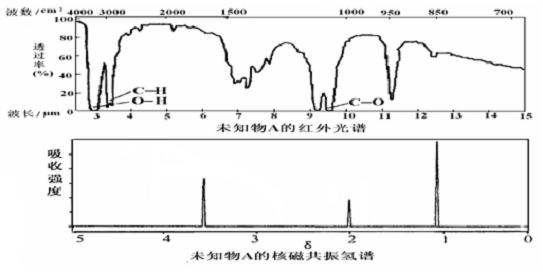

| A、由红光外谱可知,该有机物中至少有三种不同的化学键 |
| B、由核磁共振氢谱可知,该有机物分子中有三种不同化学环境的氢原子 |
| C、仅由其核磁共振氢谱无法得知其分子中的氢原子总数 |
| D、若A的化学式为C3H6O,则其结构简式为CH3CH2CHO |
已知25℃,醋酸、次氯酸、碳酸、亚硫酸的电离平衡常数如表,下列叙述正确的是( )
| 酸 | 电离平衡常数 |
| 醋酸 | Ki=1.75×10-5 |
| 次氯酸 | Ki=2.98×10-8 |
| 碳酸 | Ki1=4.30×10-7 Ki2=5.61×10-11 |
| 亚硫酸 | Ki1=1.54×10-2 Ki2=1.02×10-7 |
| A、25℃,等pH值的CH3COONa、NaClO、Na2CO3和Na2SO3四种溶液中,物质的量最小的是Na2CO3 |
| B、少量的SO2通入NaClO溶液中反应的离子方程式为:SO2+H2O+2ClO-→SO32-+2HClO |
| C、少量CO2通入Ca(ClO)2溶液中反应的离子方程式为:CO2+H2O+ClO-→HCO3-+HClO |
| D、向pH=a的醋酸溶液中加一定量水,所得溶液的pH>a、pH<a、pH=a均有可能 |
化合物M叫假蜜环菌甲素,它是香豆素类天然化合物.对M的性质叙述正确的是( )
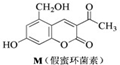

| A、M与Br2只能发生加成反应,不能发生取代反应 |
| B、M既能与FeCl3发生反应,也能与CH3COOH发生反应 |
| C、M可溶于NaOH稀溶液,1mol M最多消耗2mol NaOH |
| D、1mol M在催化剂作用下最多能与4mol H2发生加成反应 |